
【患者像】ラツーダの治療対象となる患者像は?
統合失調症では、「初発の急性期患者」や「幻覚や妄想が再燃した急性期患者」などがラツーダの治療対象となります。

解説
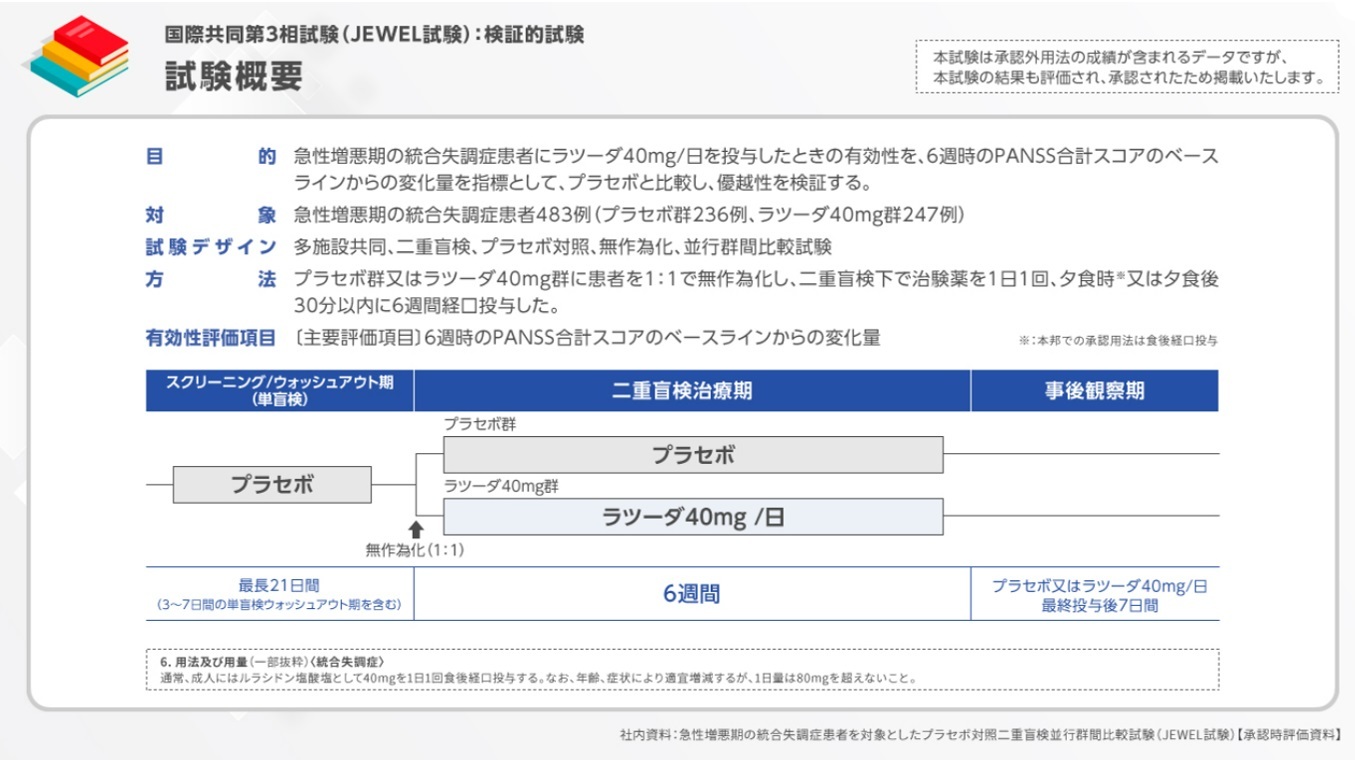

ラツーダが本邦において統合失調症の適応症を取得する根拠となった第3相試験がJEWEL試験です。
本試験の対象は、急性増悪期の統合失調症患者483例です。対象をプラセボ群又はラツーダ40mg群に無作為に分け、治験薬を1日1回、夕食時*又は夕食後に6週間経口投与しました。


有効性の主たる解析は、ITT集団を対象として実施しました。有効性の主要評価項目である6週時のPANSS合計スコアのベースラインからの変化量は、併合した実施医療機関、評価時期、治療群、治療群と評価時期の交互作用および、ベースラインのPANSS合計スコアを共変量とする反復測定のための混合モデル(MMRM)法を用いて解析し、最終評価時(LOCF)に治療効果(反応)が認められた患者の割合をLogistic regressionで評価しました。
安全性解析対象集団は、無作為化され二重盲検治療期に少なくとも1回治験薬を投与された患者として実施しました。
*:本邦での承認用法は食後経口投与
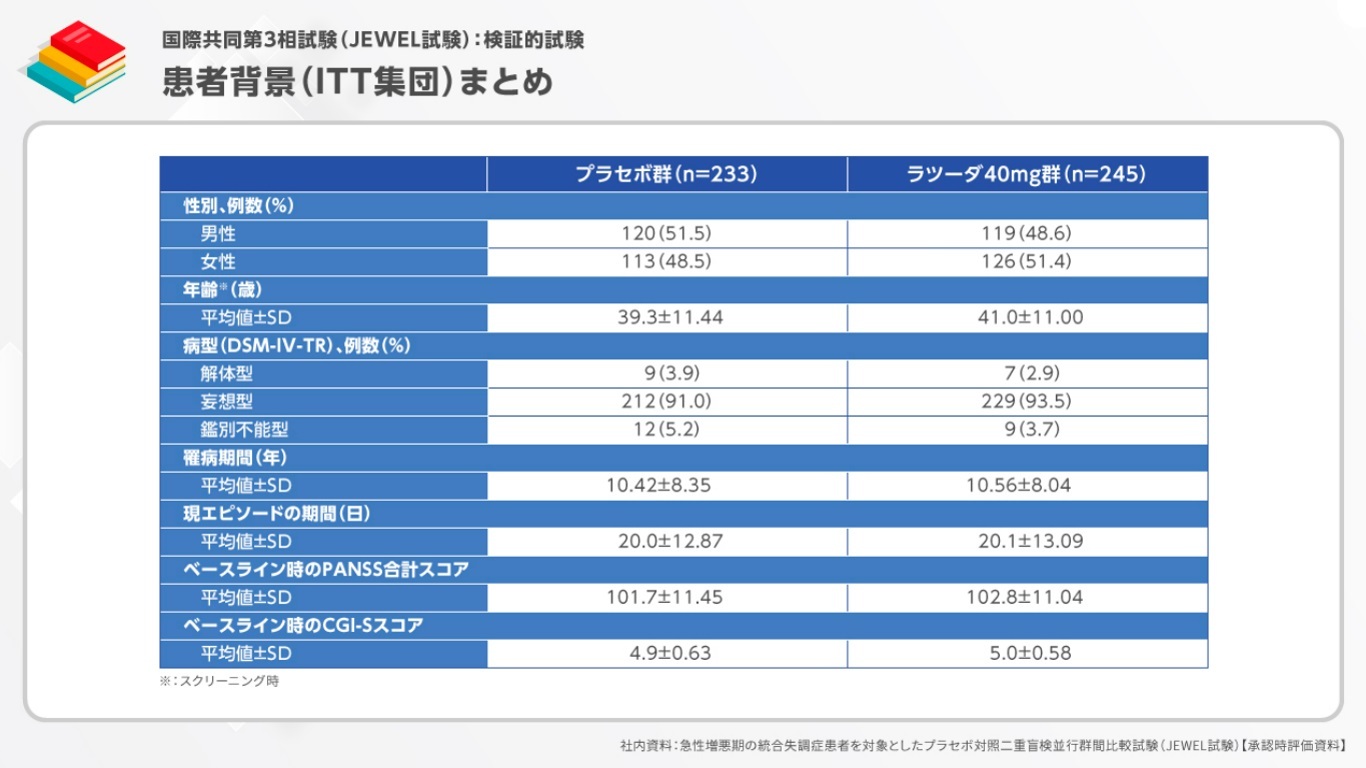

患者背景をみると、男女比は約1:1、平均年齢は約40歳でした。病型は妄想型が約90%、罹病期間は約10年、現エピソードの期間は約20日でした。
また、ベースライン時のPANSS合計スコアは、プラセボ群で101.7、ラツーダ40mg群で102.8、CGI-Sスコアはそれぞれ4.9、5.0でした。
このように、本試験には、若年で、急性期で、中等度以上の症状を有する患者が組み入れられました。
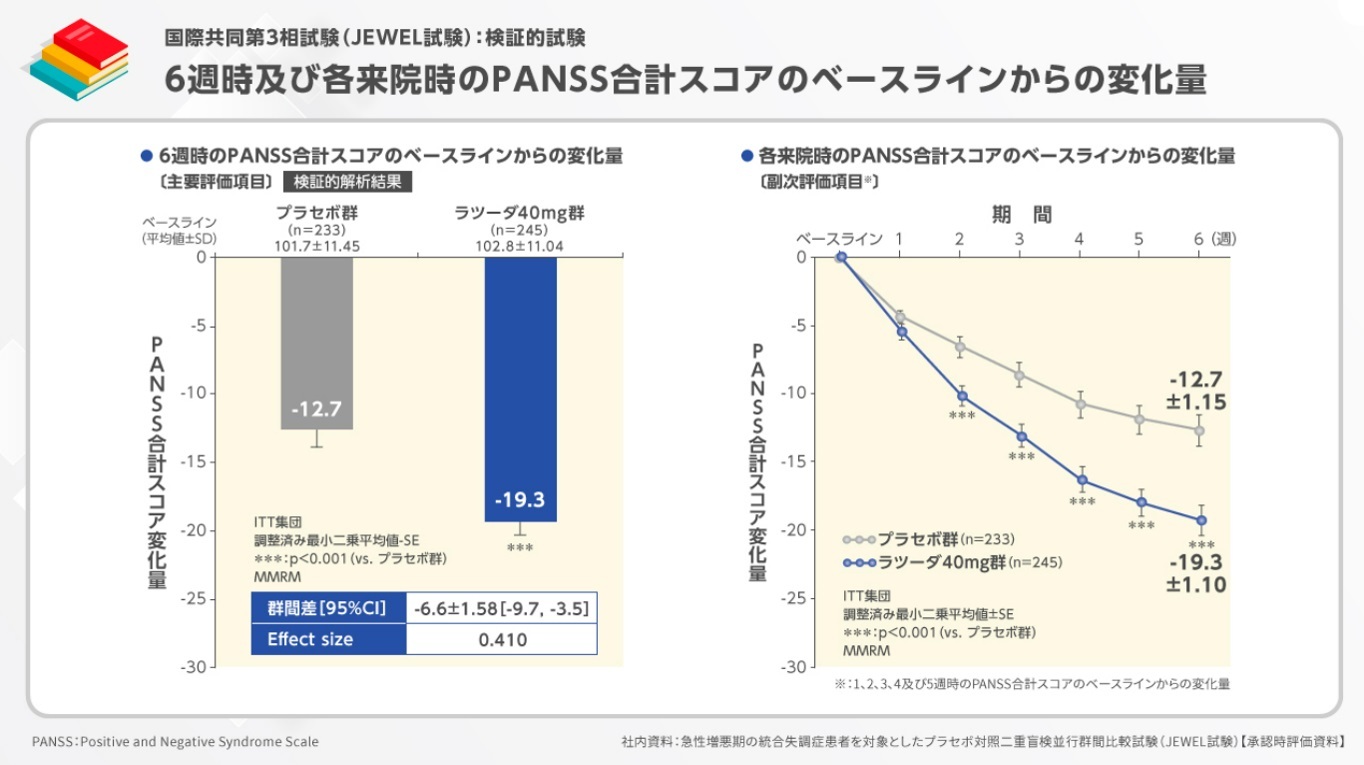

主要評価項目である6週時のPANSS合計スコアのベースラインからの変化量は、プラセボ群-12.7、ラツーダ40mg群-19.3、投与群間の差-6.6と、統計学的に有意であり、ラツーダ40mgのプラセボに対する優越性が検証されました。また、Effect sizeは0.410でした。
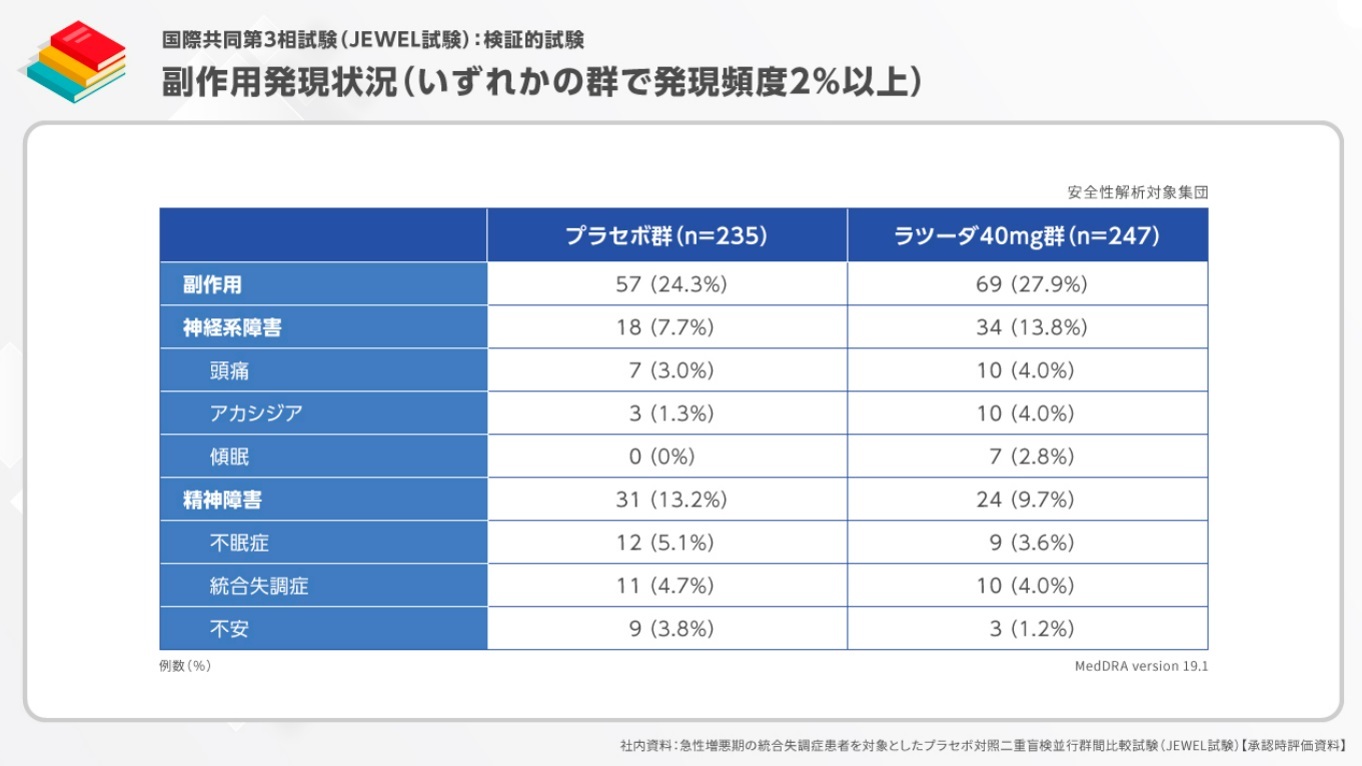

副作用発現頻度は、プラセボ群57例(24.3%)、ラツーダ40mg群69例(27.9%)でした。
発現頻度が2%以上の副作用は、プラセボ群では不眠症12例(5.1%)、統合失調症11例(4.7%)、不安9例(3.8%)などで、ラツーダ40mg群では頭痛、アカシジア、統合失調症が各10例(4.0%)などでした。
重篤な副作用は、プラセボ群2例2件[統合失調症、自殺企図各1件]、ラツーダ40mg群1例1件[統合失調症1件]に認められました。
投与中止に至った有害事象は、プラセボ群15例[統合失調症11例、手骨折、精神病性障害、敵意、自殺企図各1例]、ラツーダ40mg群14例[統合失調症7例、房室ブロック、肺結核、体重増加、不安、カタトニー、妄想、精神病性障害各1例]に認められました。
試験期間中、いずれの群においても死亡は報告されませんでした。
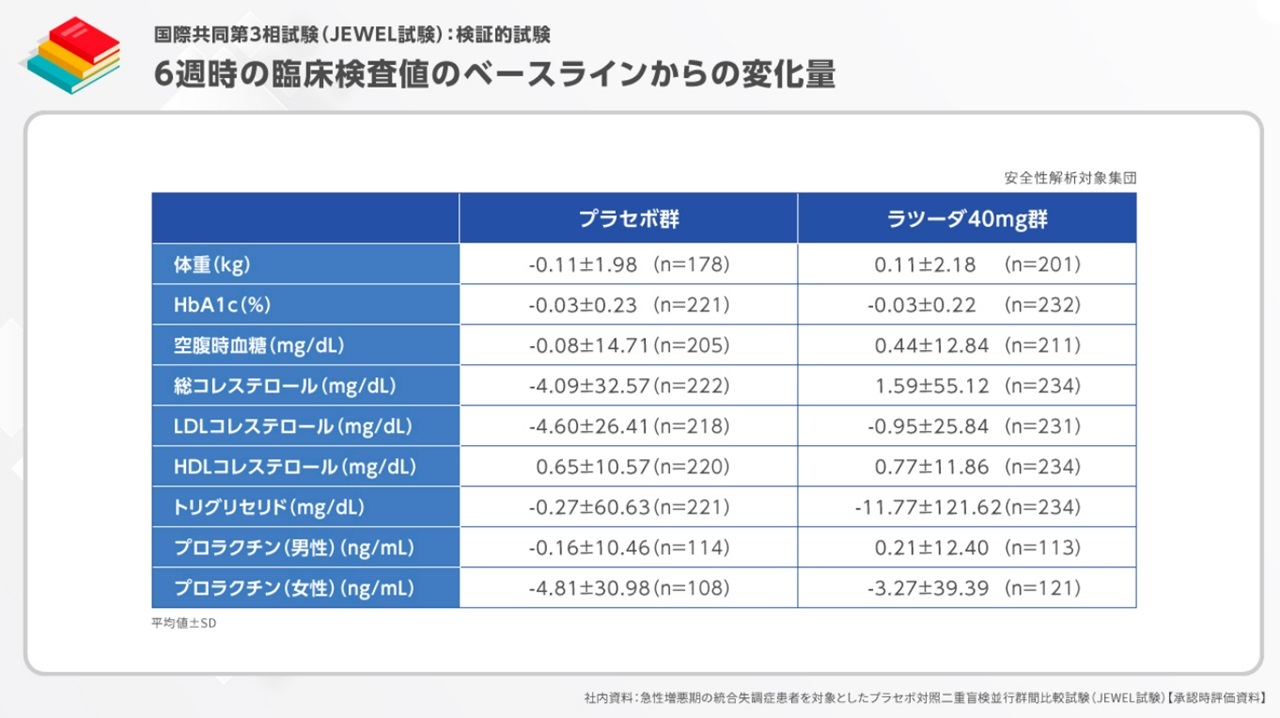

本試験では、臨床検査値への影響も検討されています。
6週時点での体重、BMIの変化量や、HbA1c、コレステロールなど糖脂質代謝への影響、プロラクチンへの影響はこちらに示す通りです。
【患者像】ラツーダの陽性症状に対する効果は?
急性増悪期の統合失調症患者を対象としたJEWEL試験では、
ラツーダ40mgは、プラセボに比べて、PANSS 5因子モデル別スコアのいずれの項目も有意に低下させました。

解説
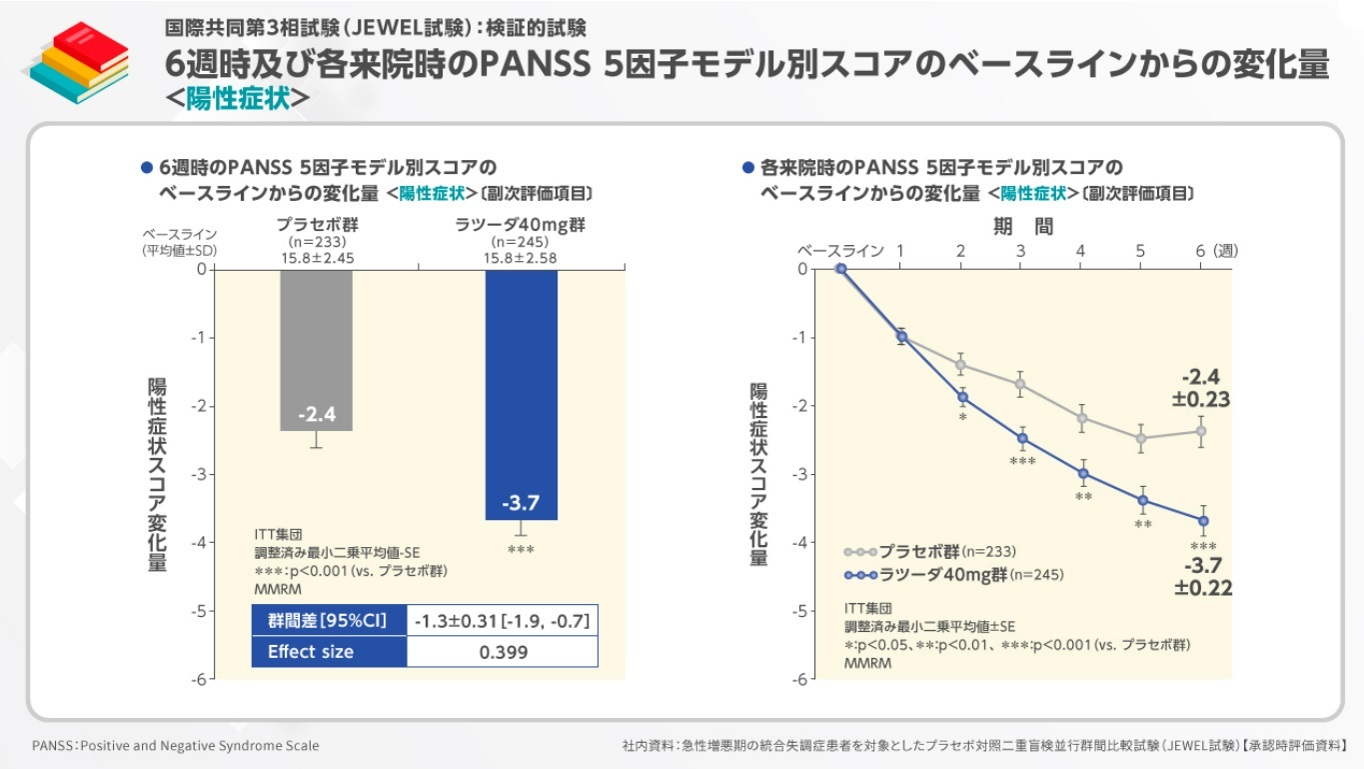

急性増悪期の統合失調症患者を対象としたJEWEL試験では、陽性症状スコアのベースラインからの変化量は、プラセボ群-2.4、ラツーダ40mg群-3.7でした。
各来院時の変化量をみると、投与開始2週目から有意差が認められました。
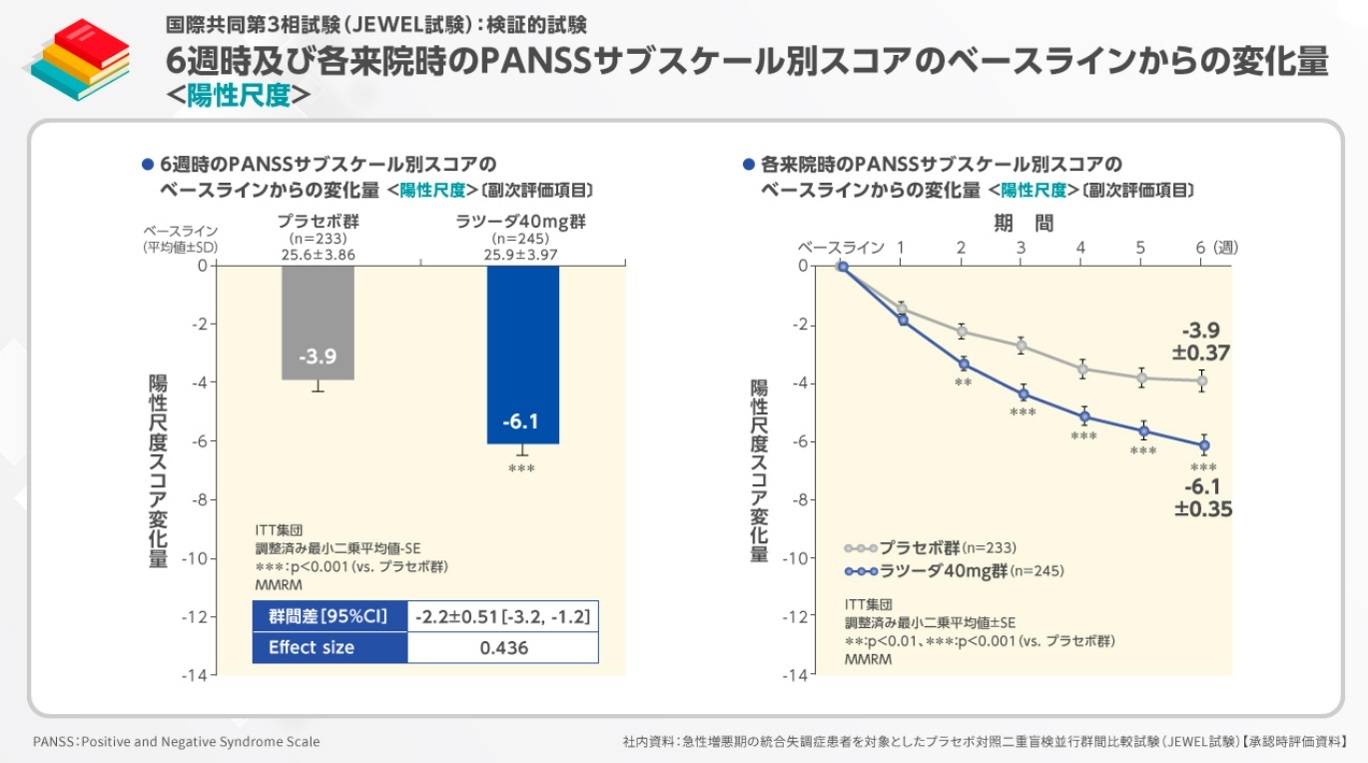

陽性尺度スコアのベースラインからの変化量は、プラセボ群-3.9、ラツーダ40mg群-6.1でした。
各来院時の変化量をみると、投与開始2週目から有意差が認められました。
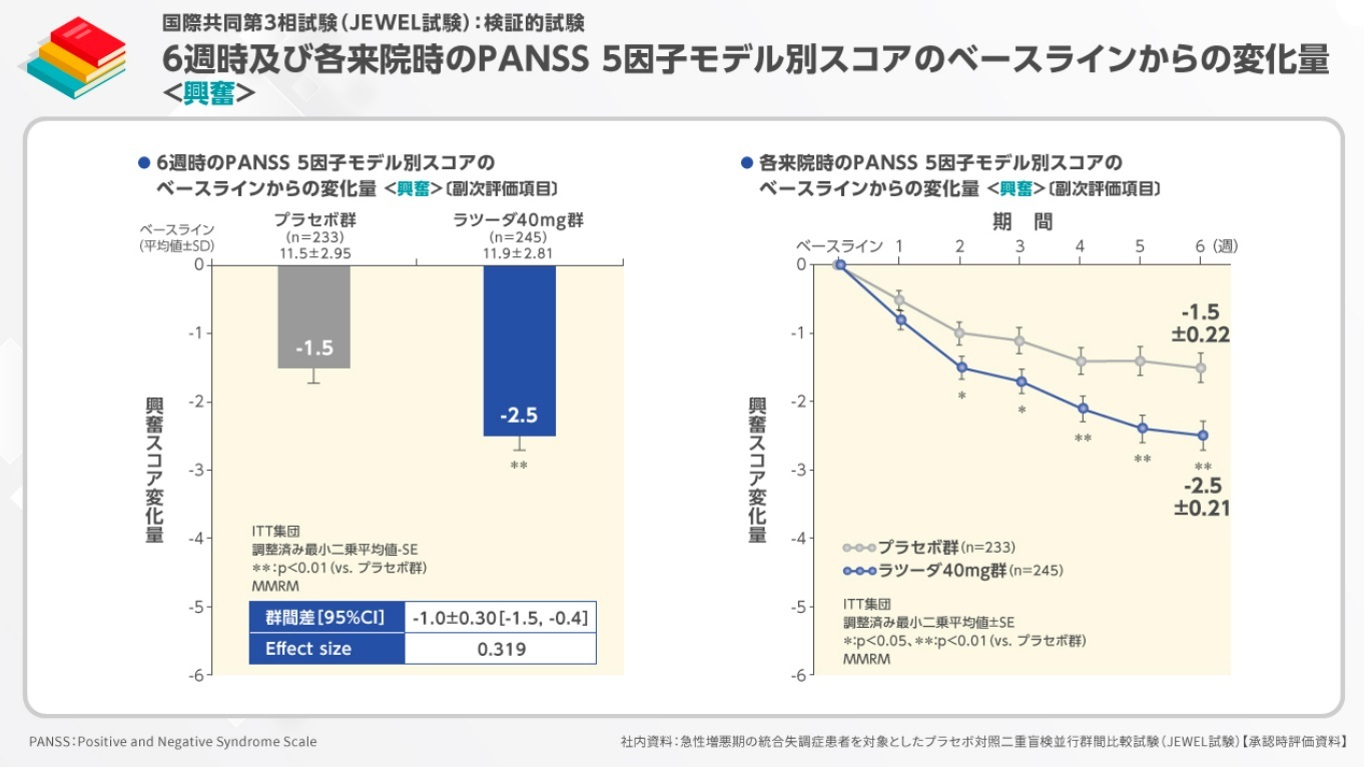

興奮スコアのベースラインからの変化量は、プラセボ群-1.5、ラツーダ40mg群-2.5でした。
各来院時の変化量をみると、投与開始2週目から有意差が認められました。
【至適用量】開始用量は何mgにすべきか?
統合失調症には、ラツーダ40mgから開始してください。

解説
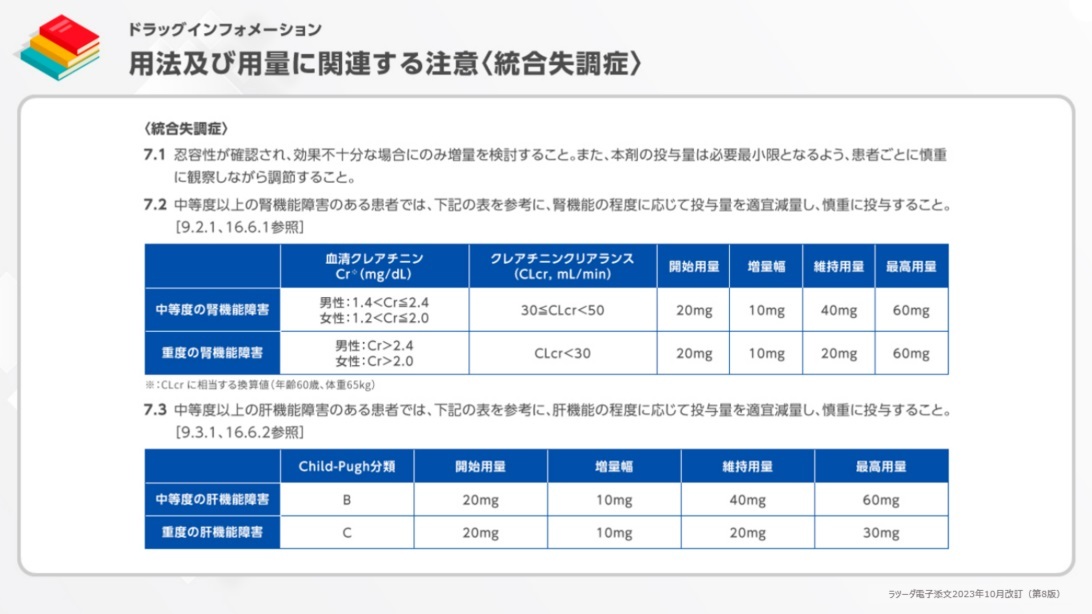

統合失調症に対する用法及び用量に関連する注意は、こちらに示す通りです。
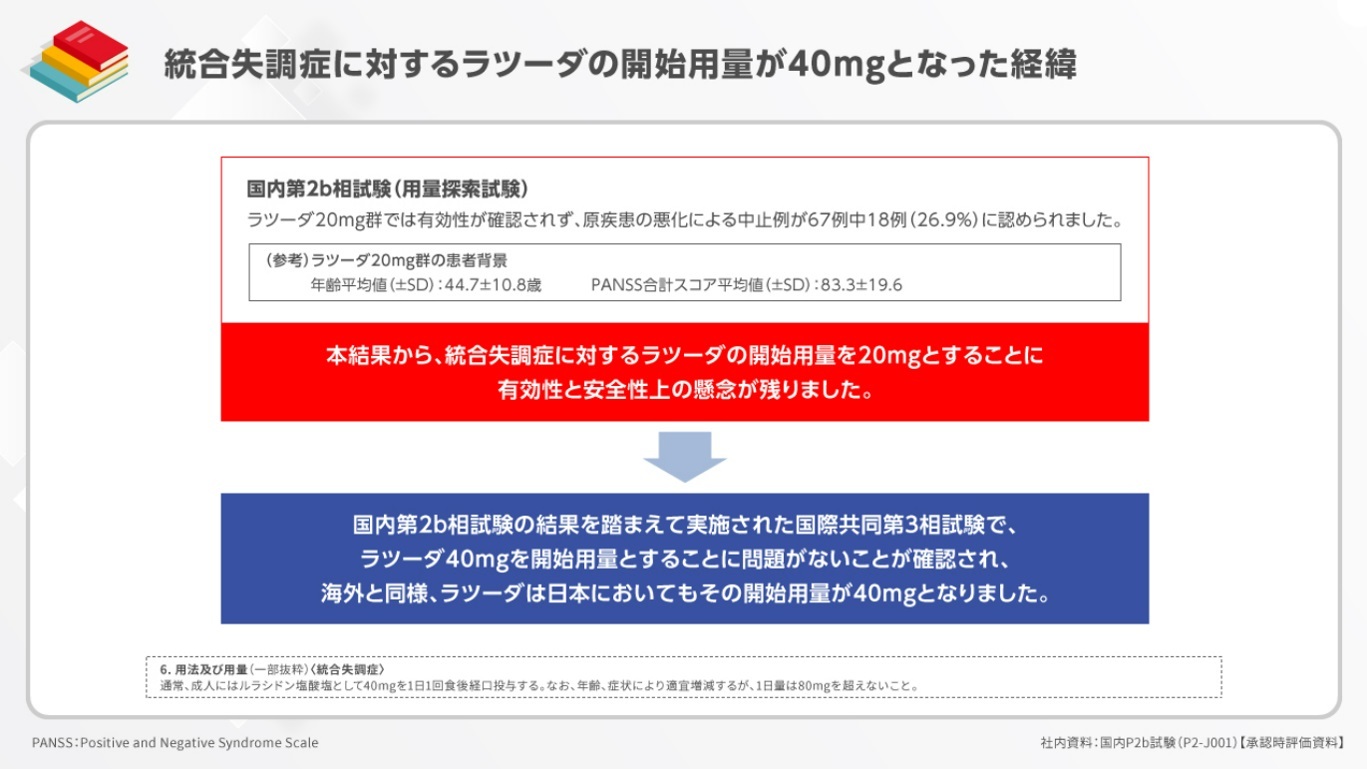

国際共同第3相試験(JEWEL試験)では、ラツーダ40mg/日が統合失調症に対する開始用量でした。この用量は、国内第2相後期試験で、20mg/日は有効性が確認できなかったばかりか、原疾患の悪化による中止が増えてしまうといった報告1)があったために設定されました。
1)社内資料:国内P2b試験(P2-J001)【承認時評価資料】
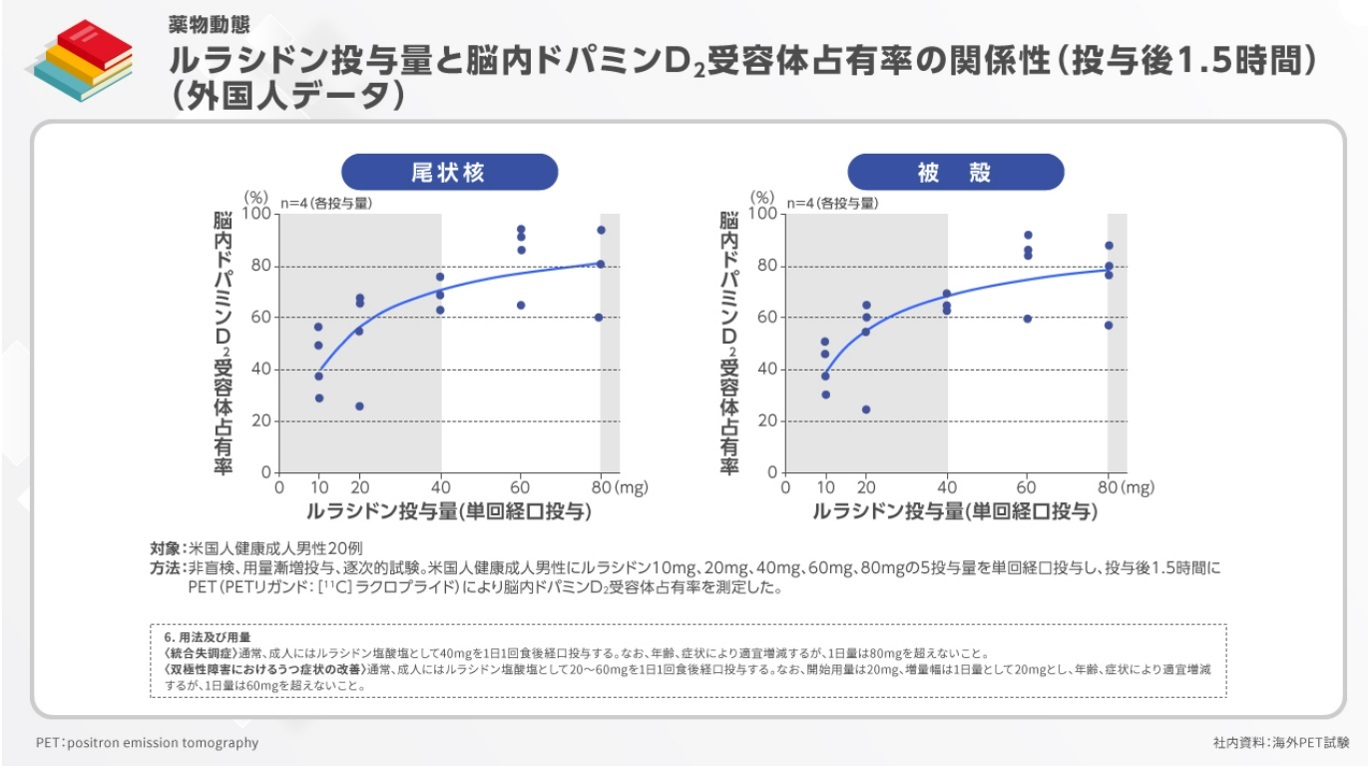

一般的に、統合失調症治療では、65%以上のドパミンD2受容体占有率が必要といわれています2)。ルラシドン投与量と脳内ドパミンD2受容体占有率の関係性を検討したグラフをみると、40mg/日がその最低ラインとなっています。つまり、承認用量の40mg~80mgが、有効性が示され副作用が出にくいとされる、いわゆるtherapeutic windowの範囲であることがわかります。
2)Nord M, et al. CNS Neurosci Ther. 2011;17(2):97-103.
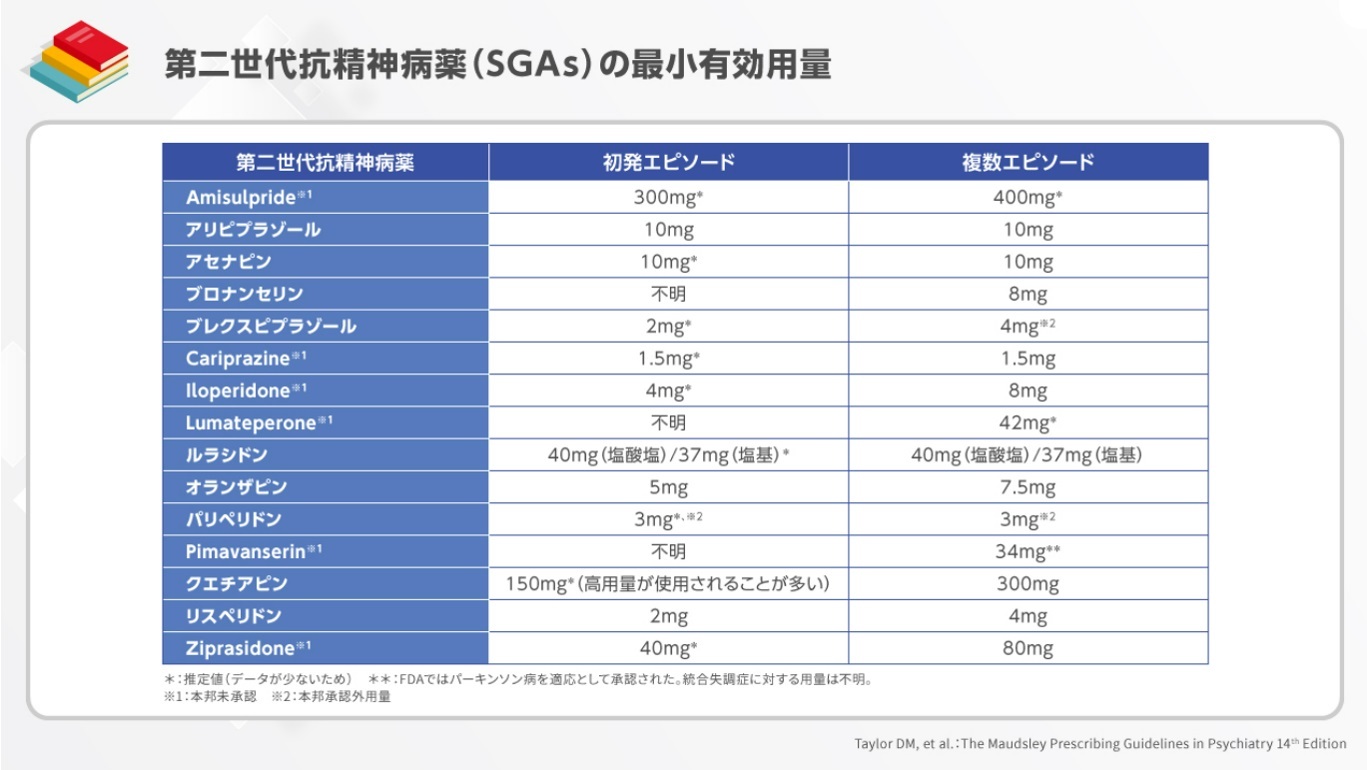

また、モーズレイ処方ガイドライン(第14版)では、ラツーダ(ルラシドン塩酸塩)の最小有効用量は、初発エピソード・複数エピソードともに、40mgと位置付けられています3)。
3)Taylor DM, et al.:The Maudsley Prescribing Guidelines in Psychiatry 14th Edition
【至適用量】80mgへの増量効果は?
JEWEL継続試験では、ラツーダ40mg群において十分な効果が得られなかった
患者集団におけるラツーダ80mg/日への増量効果が検討されました。
その結果、PANSS合計スコアがベースラインから20%以上改善しなかった患者集団における
PANSS合計スコア変化量は、ラツーダ最頻投与量40mg群では-6.2、80mg群では-10.7でした。

解説
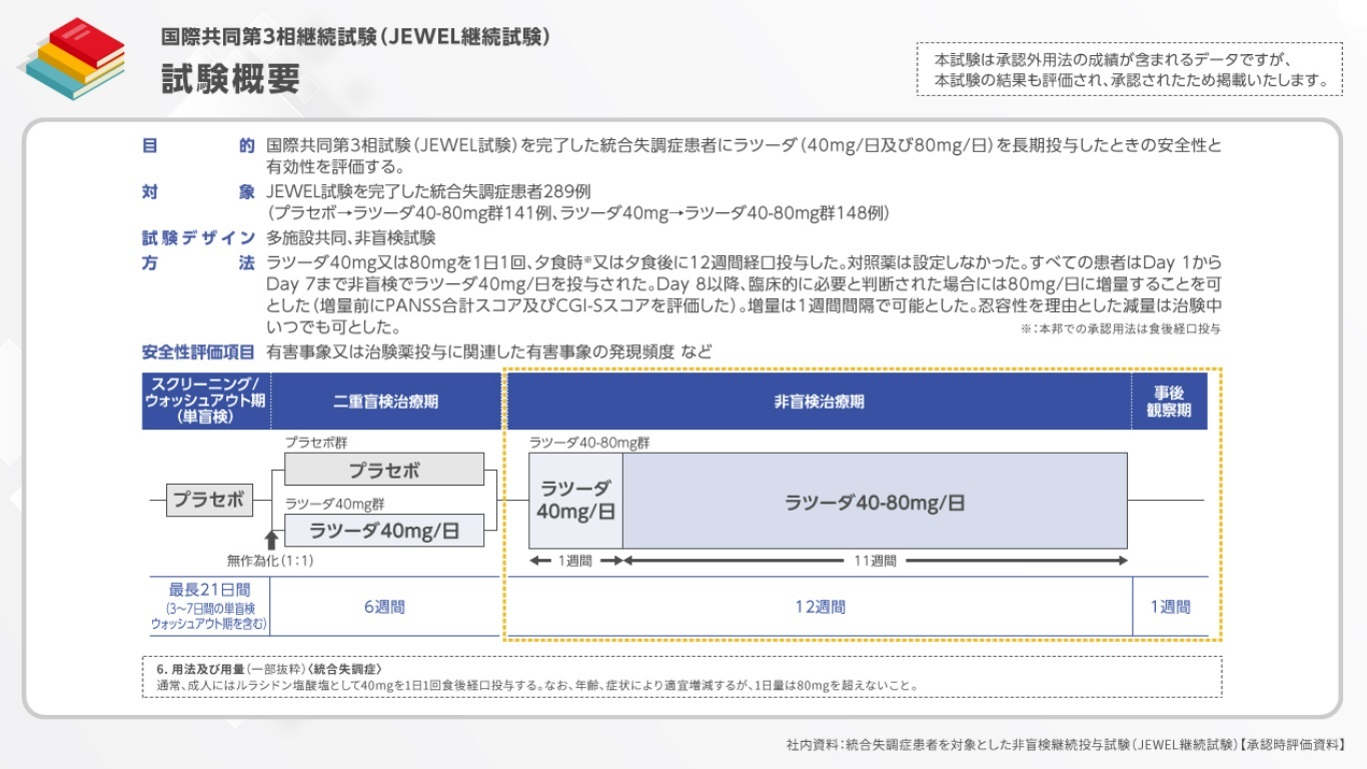

国際共同第3相試験(JEWEL継続試験)では、JEWEL試験を完了した統合失調症患者にラツーダ(40mg/日及び80mg/日)を長期投与したときの安全性と有効性を評価しました。
対象は、先行試験であるJEWEL試験を完了した統合失調症患者289例です。

12週間の非盲検治療期では、ラツーダ40mg又は80mgを1日1回、夕食時*又は夕食後に経口投与しました。Day 1からDay 7まではラツーダ40mg/日を投与し、Day 8以降は、臨床的に必要と判断された場合には80mg/日に増量することを可としました。
*:本邦での承認用法は食後経口投与
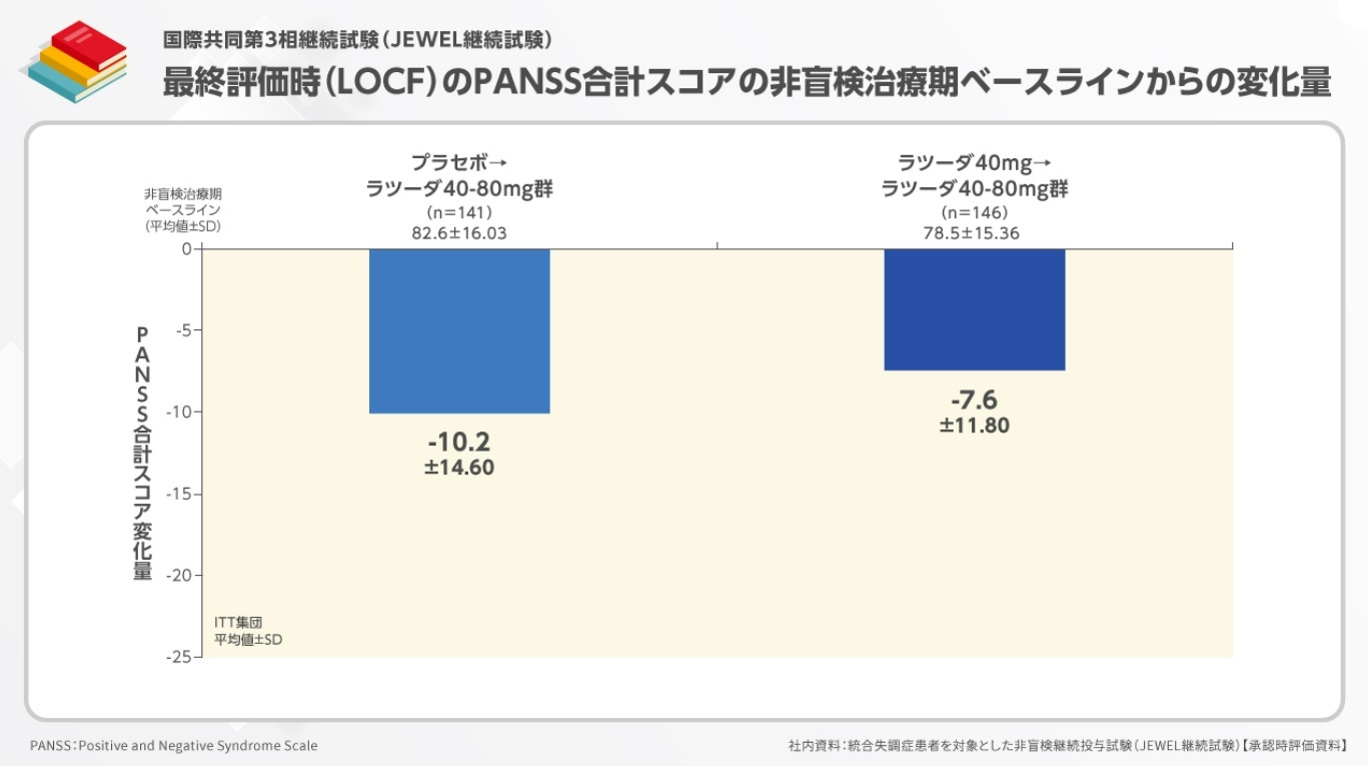

最終評価時(LOCF)のPANSS合計スコアの非盲検治療期ベースラインからの変化量は、プラセボ→ラツーダ40-80mg群-10.2、ラツーダ40mg→ラツーダ40-80mg群-7.6でした。
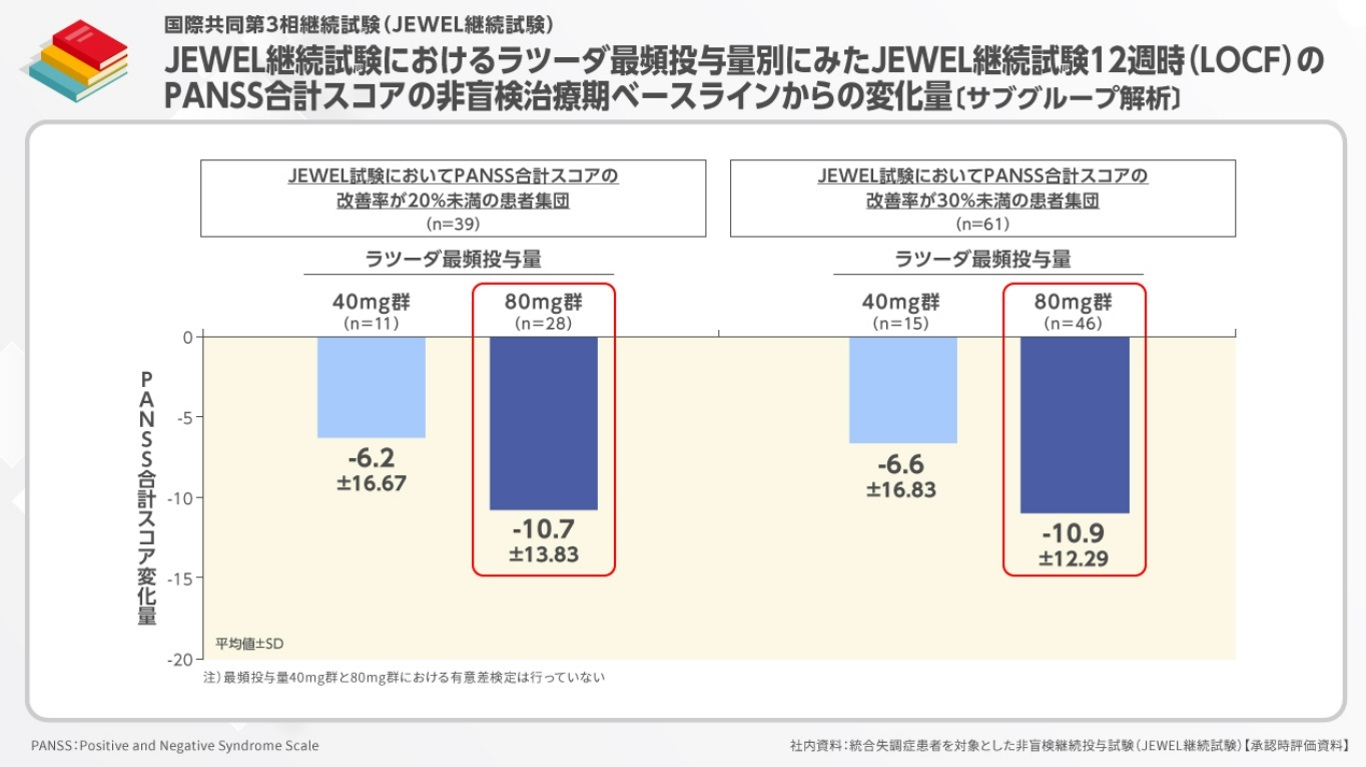

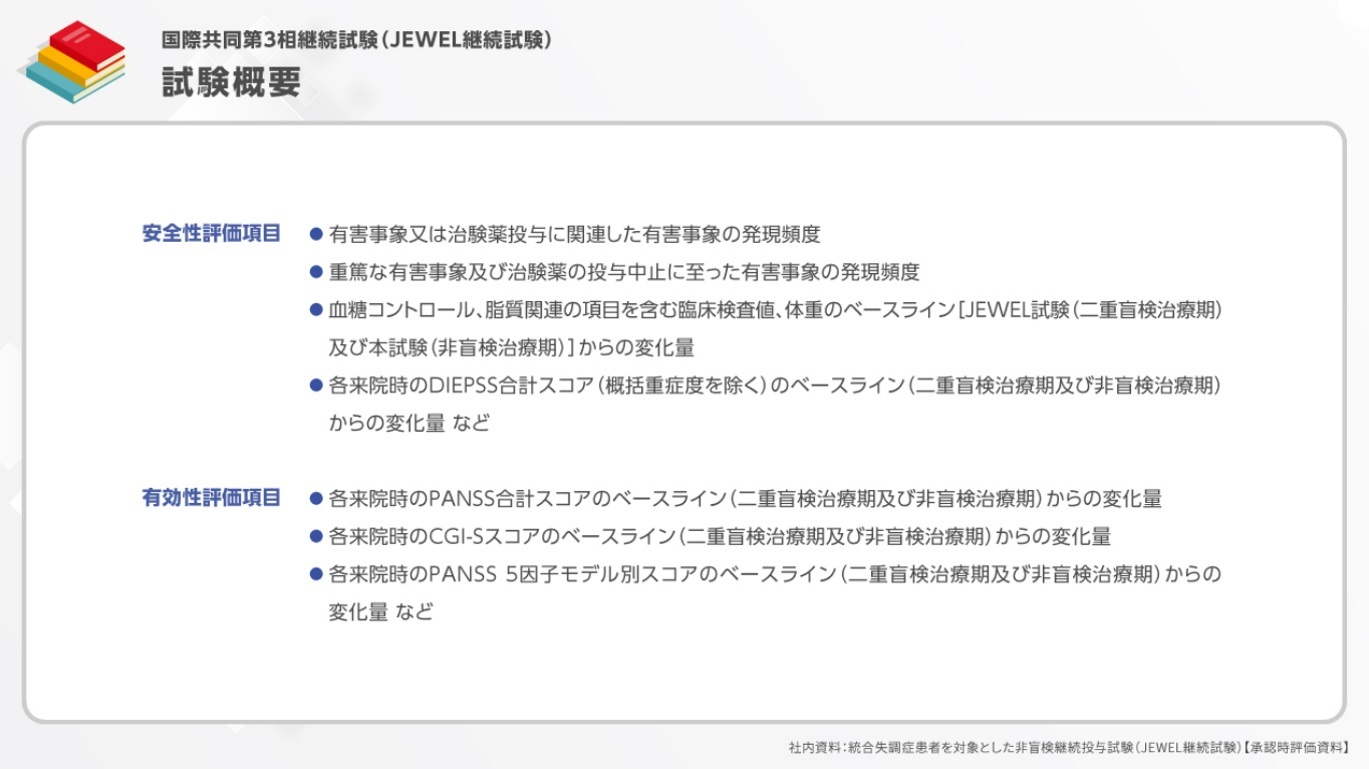
また、サブグループ解析では、JEWEL試験のラツーダ40mg群において、十分な効果が得られなかった患者集団におけるラツーダ80mg/日への増量効果が検討されました。その結果、PANSS合計スコアがベースラインから20%以上改善しなかった患者集団におけるPANSS合計スコア変化量は、ラツーダ最頻投与量40mg群では-6.2、80mg群では-10.7でした。また、PANSS合計スコアがベースラインから30%以上改善しなかった患者集団では、それぞれ-6.6、-10.9でした。
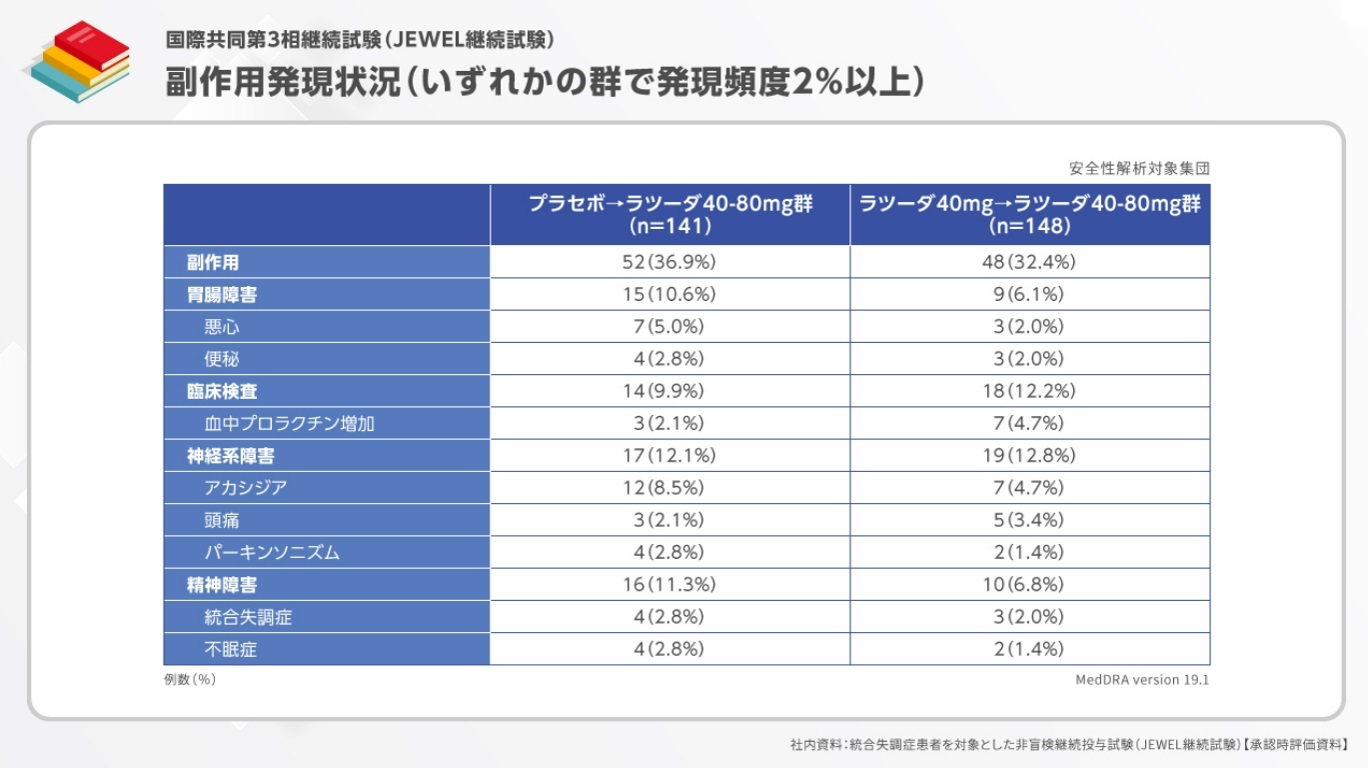

副作用発現頻度は、プラセボ→ラツーダ40-80mg群36.9%、ラツーダ40mg→ラツーダ40-80mg群32.4%でした。いずれかの群で発現頻度が2%以上であった副作用は、プラセボ→ラツーダ40-80mg群、ラツーダ40mg→ラツーダ40-80mg群の順に、悪心5.0%、2.0%、便秘2.8%、2.0%、血中プロラクチン増加2.1%、4.7%、アカシジア8.5%、4.7%、頭痛2.1%、3.4%、パーキンソニズム2.8%、1.4%、統合失調症2.8%、2.0%、不眠症2.8%、1.4%でした。
重篤な副作用は、プラセボ→ラツーダ40-80mg群5例6件[統合失調症4件、衝動行為、自殺企図各1件]、ラツーダ40mg→ラツーダ40-80mg群3例3件[統合失調症3件]に認められました。
投与中止に至った有害事象は、プラセボ→ラツーダ40-80mg群10例[統合失調症6例、アラニンアミノトランスフェラーゼ増加、QT延長、背部痛、衝動行為各1例]、ラツーダ40mg→ラツーダ40-80mg群8例[統合失調症5例、不安、血管浮腫、蕁麻疹各1例]でした。
なお、試験期間中、いずれの群においても死亡は報告されませんでした。
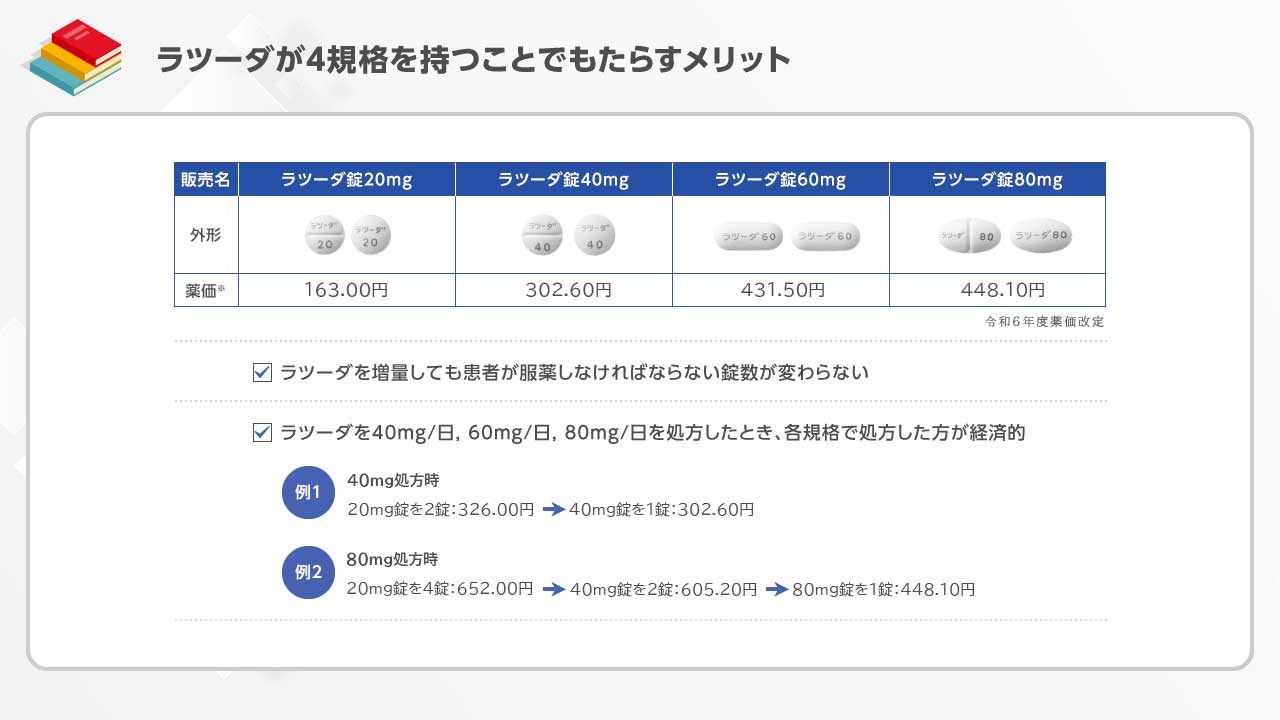

なお、ラツーダは、20mg、40mg、60mg、80mgの4規格あります。ラツーダを40mg/日、60mg/日、80mg/日を処方する際は、各規格で処方した方が経済的です。
ラツーダの臨床疑問 まとめ
ラツーダは、急性増悪期の統合失調症患者さんに有用性が示されています。
また、統合失調症におけるラツーダの開始用量は40mgで、症状に応じて最大80mgまで増量することが可能です。。

エキスパートが解説!ラツーダ MOVIE LIBRARY


