第11回 受容体特性から考える抗精神病薬の使い方とラツーダへの期待

本シリーズでは、精神科医療で先進的な取り組みを行っている施設の先生に、施設の特徴や治療方針、ラツーダへの期待などをお伺いします。
今回は、東京慈恵会医科大学 精神医学講座 客員教授/医療法人社団光生会 平川病院 副院長の宮田 久嗣先生に、受容体特性から考える抗精神病薬の使い方とラツーダへの期待をご解説いただきます。
東京慈恵会医科大学 精神医学講座の特徴と地域における役割

基幹病院となる東京慈恵会医科大学附属病院の精神神経科は、東京23区内の大学病院の精神神経科としては数少ない開放および閉鎖病床のある入院病棟(49床)を有しており、隔離室3床を確保しています。東京都港区に位置する都市型の大学病院ということもあり、20~50代の働き世代の方たちが、ストレスによる精神疾患や職場のうつ病などで受診されることが比較的多いです。実際、2019年の外来患者さん(初診)の疾患割合をみると、ストレス障害が最も多く、次いで感情障害、術前・術後の他科依頼、統合失調症でした。
依存と嗜癖とは
依存・嗜癖は私の専門分野ですが、嗜癖(addiction)と依存(dependence)ほど紆余曲折を経てきた精神科用語は珍しいかもしれません。その背景には、さまざまな種類の物質が乱用されてきたこと、加えて最近は、物質だけではなく、ギャンブルやゲームなどの行動も共通の疾病カテゴリーで考えられるようになったことなどが関係しています。依存は、物質に対して用いられる用語ですので、ギャンブルやゲームのような行動には使用できません。一方、嗜癖はギャンブルやゲームのような行動に対して用いることができます。これらの嗜癖と依存の関係を一言でいうならば、嗜癖の中で、物質使用によって生じた特定の状態が依存ということになります。
最近の嗜癖に関するトピックスのひとつに、「共存しながらのコントロール」があります。たとえば、スマートフォンの使用です。覚醒剤などは、“百害あって一利なし”なので断薬(やめること)を治療目標としますが、スマートフォンは、ゲームや課金などの嗜癖行動の要因となる一方、生活必需品でもあるため、完全になくすことはできません。このような、最近増えているゲームや課金などの嗜癖行動は、共存しながらコントロールしていくことが重要なのです。
各種受容体と想定される抗精神病薬の臨床効果
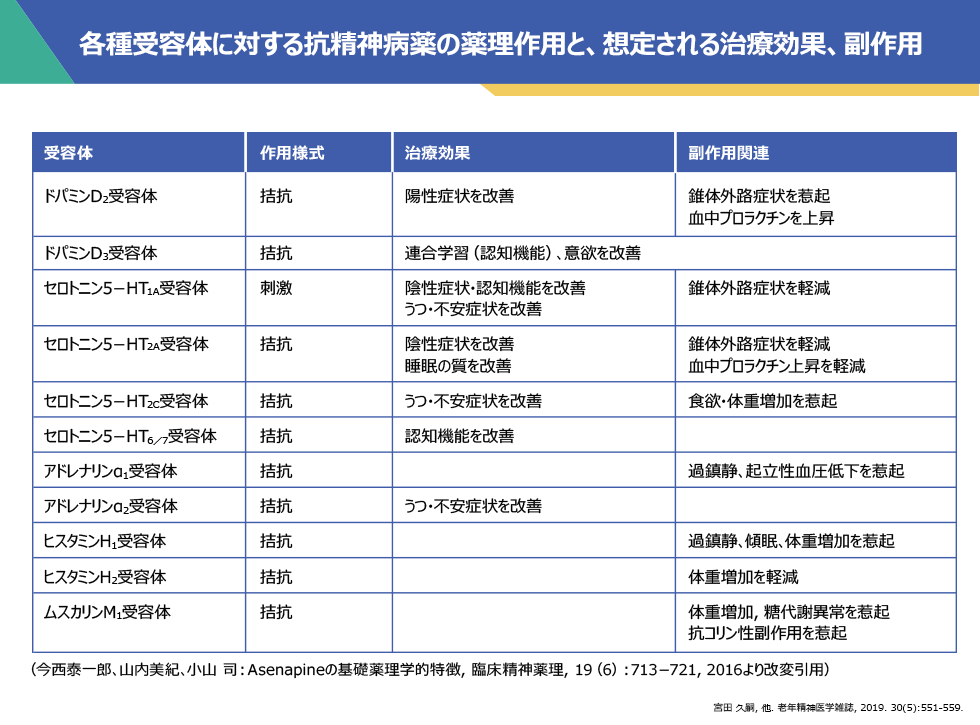
抗精神病薬は、主として統合失調症の幻覚妄想や精神運動興奮に使用されますが、双極性障害やうつ病の気分症状にも用いられます。この抗精神病薬は、作用する各種受容体ごとに想定される治療効果や副作用が異なります。
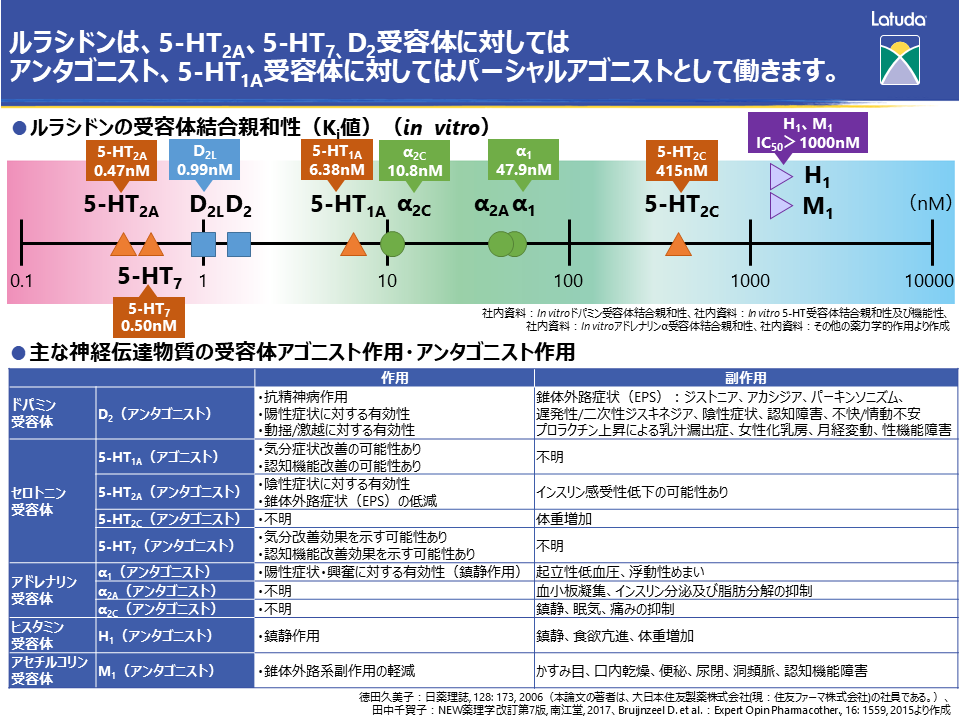
ドパミン受容体では、D2受容体の遮断によって幻覚、妄想などの陽性症状は改善するものの、運動系の副作用(錐体外路症状)や内分泌系の副作用(血中プロラクチン上昇と性機能障害)が生じます。D3受容体の遮断では、快(報酬)に関連した連合学習の促進と、これに基づく動機づけ(意欲)の改善が期待されます。
セロトニン受容体に関しては、5-HT1A受容体の刺激によって陰性症状や認知機能の一部改善、うつ・不安の改善、および錐体外路性副作用の軽減が報告されています。5-HT2A受容体の遮断によって陰性症状の一部改善や睡眠の改善のほか、副作用である錐体外路症状や血中プロラクチン上昇の改善効果が期待されます。また、5-HT6/7受容体遮断では、動物実験のレベルではありますが、認知機能の改善が報告されています。

受容体特性から考える抗精神病薬の使い方
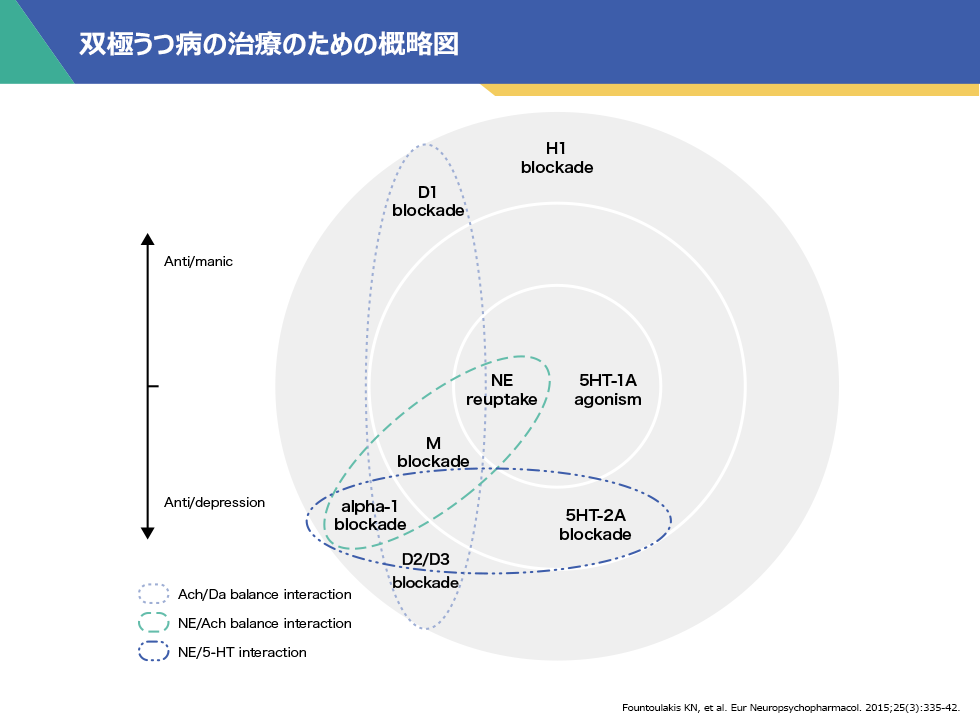
双極性障害におけるうつ症状とうつ病の治療は分けて考えることが重要です。ガイドラインでも、双極性障害の抑うつエピソードに対して、抗うつ薬を単独で用いることは推奨されていません1)。これは、双極性障害うつ症状の病態を受容体の観点から説明することができます。うつ病では、セロトニンとノルアドレナリンが低下していると考えられています。一方、双極性障害うつ症状は、セロトニンやノルアドレナリンに加えて、ドパミン、ヒスタミン、ムスカリンが複雑に関与しているのではないかと考えられています。そのため、双極性障害うつ症状には、セロトニンやノルアドレナリンにのみ作用するような抗うつ薬は効果が期待しにくいのです。このような受容体特性の観点から、双極性障害うつ症状には、セロトニン、ノルアドレナリン、ドパミン、ヒスタミン、ムスカリンに作用する抗精神病薬を使うことが合理的と考えられます。
1)日本うつ病学会 気分障害の治療ガイドライン作成委員会:日本うつ病学会治療ガイドラインⅠ.双極性障害 2020, 2020年6月16日第4回改訂,p11-13.

ラツーダへの期待

統合失調症患者さんを対象としたJEWEL試験では、PANSS合計スコアのベースラインからの変化量は、ラツーダ40mg群で投与2週目よりプラセボ群と有意差が認められました。さらに、PANSS 5因子モデル別スコアのベースラインからの変化量については、急性期で特に問題となる陽性症状をはじめ、興奮、陰性症状、不安/抑うつ、認知障害のいずれの項目においても、ラツーダはプラセボに比べてスコアを有意に低下させました。この結果から、ラツーダは、統合失調症の患者さんの幅広い症状に有効であることが示唆されました。
なお、JEWEL試験における副作用発現頻度は、プラセボ群57例(24.3%)、ラツーダ40mg群69例(27.9%)でした。発現頻度が2%以上の副作用は、プラセボ群では不眠症12例(5.1%)、統合失調症11例(4.7%)、不安9例(3.8%)などで、ラツーダ40mg群では頭痛、アカシジア、統合失調症が各10例(4.0%)などでした。重篤な有害事象は、プラセボ群2例2件[統合失調症、自殺企図各1件]、ラツーダ40mg群1例1件[統合失調症1件]に認められました。投与中止に至った有害事象は、プラセボ群15例[統合失調症11例、手骨折、精神病性障害、敵意、自殺企図各1例]、ラツーダ40mg群14例[統合失調症7例、房室ブロック、肺結核、体重増加、不安、カタトニー、妄想、精神病性障害各1例]に認められました。試験期間中、いずれの群においても死亡は報告されませんでした。
双極性障害患者さんを対象としたELEVATE試験においては、MADRS合計スコアのベースラインからの変化量は、ラツーダ20-60mg群では投与開始2週目よりプラセボと比べ有意な改善が認められました。私の実臨床での印象も同様で、2~3週間程度の速やかな効果発現が期待できると感じています。また、ELEVATE試験は長期投与試験も行われています。ELEVATE長期試験では、日本人集団(ELEVATE試験を完了した患者)において、ラツーダ20-60mg→ラツーダ20-120mg群(ラツーダ120㎎は承認外用量です)における52週時及び最終評価時(LOCF)のMADRS合計スコアの二重盲検治療期ベースラインからの変化量は、 それぞれ−25.7、−14.8でした。 双極性障害におけるうつ症状は、再発しやすい疾患ですので、このように長期にわたる有効性が検討されている点を評価しています。
また、JEWEL試験、ELEVATE試験における臨床検査値への影響をみると、長期を見据えた治療に適していると考えられます。特に、認知機能の低下が生活上の支障になる就学や就労にかかわる世代の患者さんの選択肢になるのではないかと期待しています。

実臨床におけるラツーダの使い方のポイント
前治療薬に鎮静効果がある場合、短期間でラツーダに切り替えると、一時的に不安定になることがあるので、慎重に切り替えていきます。私は、ラツーダを上乗せして、前治療薬を漸減していきます。
ラツーダは抗コリン作用が弱い点で副作用上のメリットがありますが、抗コリン作用の強い薬剤から切り替える場合には、コリン作動性の離脱症状(不安、焦燥など)に注意しながら、時間をかけて前治療薬を減らすことが推奨されます。
ELEVATE試験
ここから、本邦において双極性障害うつ症状の改善の適応症を 取得する根拠となった第3相試験、ELEVATE試験をご紹介いたします。
試験概要
本試験の対象は、双極Ⅰ型障害患者(大うつ病エピソード)525例です。対象をプラセボ群、ラツーダ20-60mg群、ラツーダ80-120mg*群に無作為に分け、治験薬を1日1回夕食後に6週間経口投与しました。
注)ラツーダ80-120mgは承認外用量です。
有効性の主たる解析はITT集団を対象として実施しました。有効性の主要評価項目は治療群、評価時期、実施医療機関、MADRS合計スコアのベースライン値、および治療群と評価時期の交互作用を含むMMRM法を用いて解析し、検定の多重性はHochberg法で調整しました。
安全性の解析は安全性解析対象集団を対象として実施しました。






有効性
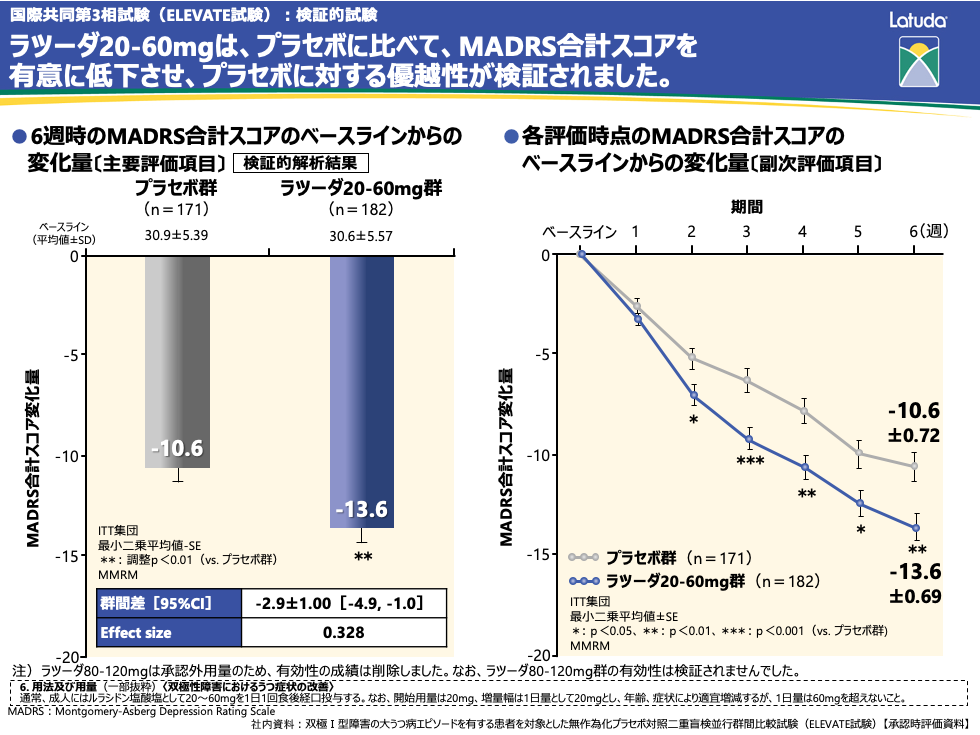
主要評価項目である6週時のMADRS合計スコアのベースラインからの変化量は、プラセボ群−10.6、ラツーダ20-60mg群−13.6、投与群間の差−2.9と、ラツーダ20-60mgはプラセボに比べてMADRS合計スコアを有意に低下させ、プラセボに対する優越性が検証されました。
また、副次評価項目であるベースラインからの変化量は、ラツーダ20-60mg群では投与開始2週目よりプラセボと比べ有意な改善が認められました。

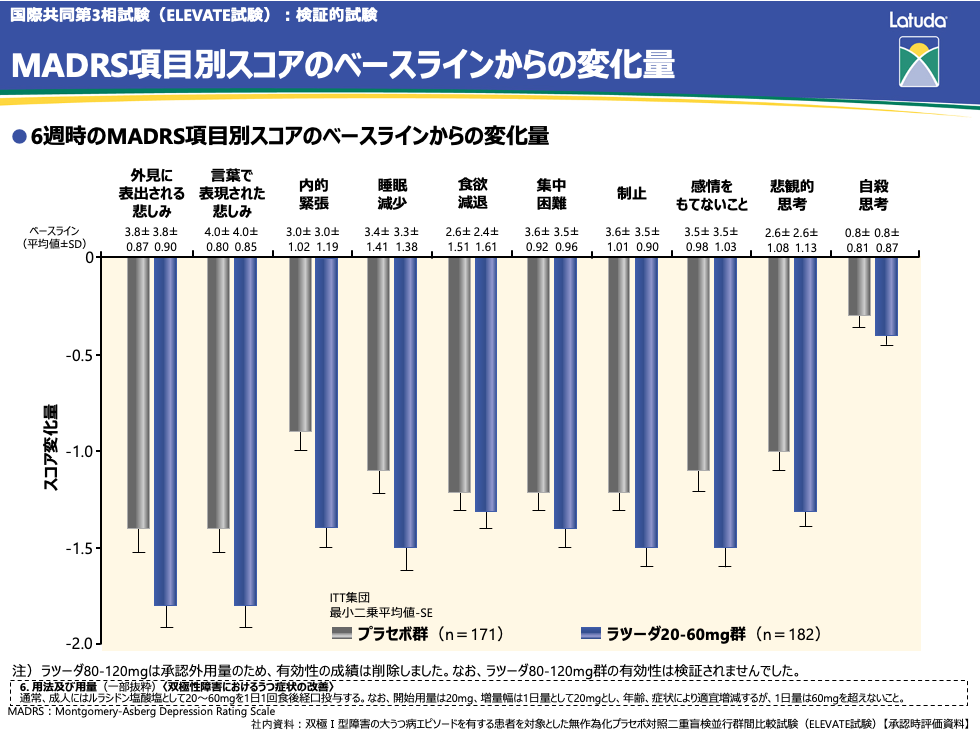
MADRS項目別スコアのベースラインからの変化量をお示しします。うつ症状の中核症状である「外見に表出される悲しみ」や「言葉で表現された悲しみ」など、各項目のスコア変化量はこちらに示すとおりです。

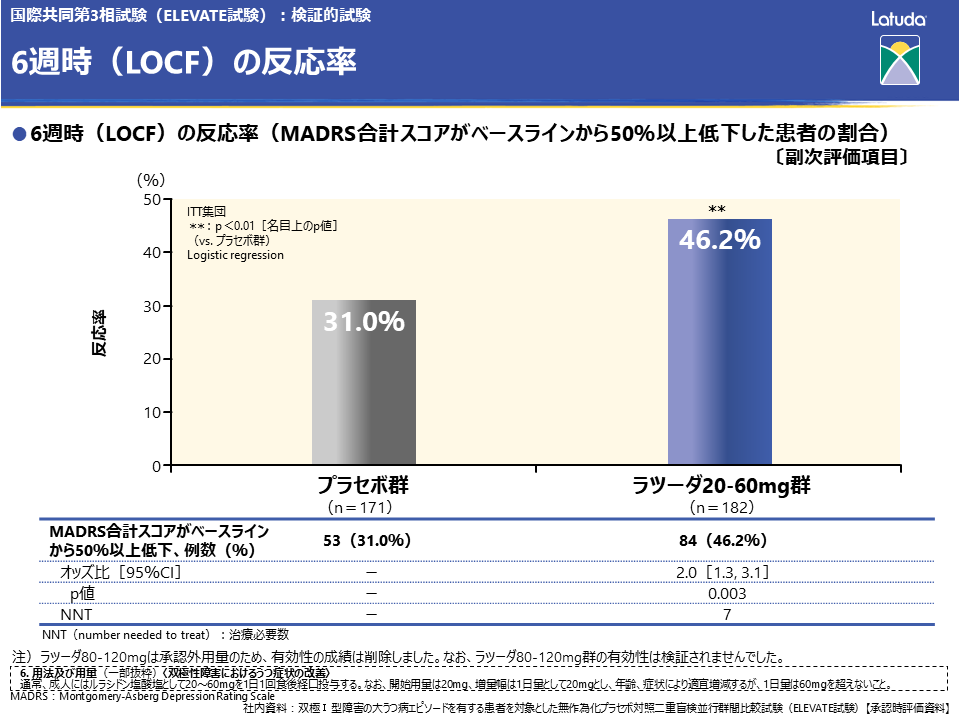
反応率は、MADRS合計スコアがベースラインから50%以上低下した患者さんの割合と定義され、6週時(LOCF)における反応率は、プラセボ群31.0%、ラツーダ20-60mg群46.2%でした。ラツーダ20-60mg群のプラセボ群に対するオッズ比は2.0、p値は0.01未満であり、ラツーダ20-60mg群のMADRS合計スコア反応率は、プラセボ群に比べて有意に高いことが示されました。なお、NNTは7でした。

安全性
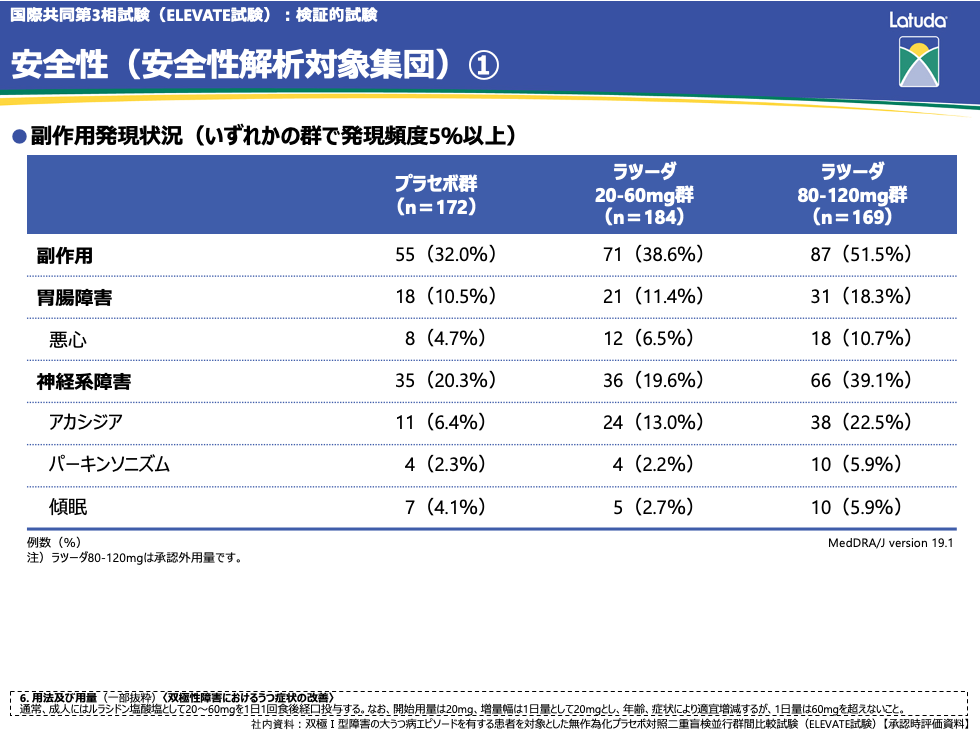
副作用発現頻度は、プラセボ群55例(32.0%)、ラツーダ20-60mg群71例(38.6%)、ラツーダ80-120mg群87例(51.5%)でした。
発現頻度5%以上の副作用は、プラセボ群ではアカシジア11例(6.4%)、悪心8例(4.7%)、ラツーダ20-60mg群ではそれぞれ24例(13.0%)、12例(6.5%)、ラツーダ80-120mg群ではそれぞれ38例(22.5%)、18例(10.7%)でした。
重篤な有害事象は、プラセボ群1例1件[躁病1件]、ラツーダ20-60mg群0例、ラツーダ80-120mg群2例2件[自殺企図、パニック発作各1件]に認められました。
投与中止にいたった有害事象は、プラセボ群7例[好中球減少症、急性心筋梗塞、胃炎、悪心、嘔吐、疾患進行、アカシジア各1例]、ラツーダ20-60mg群6例[嘔吐、機能性胃腸障害、肝障害、アカシジア、躁病、自殺念慮各1例]、ラツーダ80-120mg群16例[悪心4例、疾患進行、アカシジア各3例、嘔吐、腱断裂、筋骨格硬直、ジストニア、不眠症、呼吸困難各1例]に認められました。
試験期間中、いずれの群においても死亡は報告されませんでした。

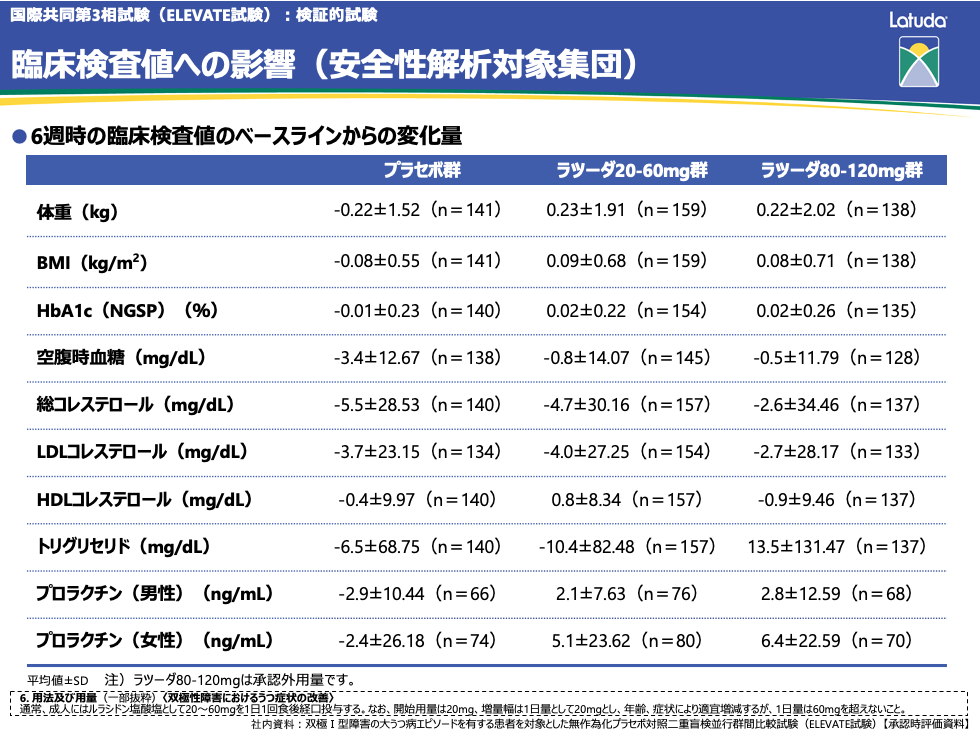
本試験では臨床検査値への影響も検討されています。6週時の体重のベースラインからの変化量は、プラセボ群−0.22kg、ラツーダ20-60mg群0.23kg、ラツーダ80-120mg群0.22kgでした。血糖に関しては、HbA1cが、プラセボ群−0.01%、ラツーダ20-60mg群0.02%、ラツーダ80-120mg群0.02%でした。