第2回 桶狭間病院 藤田こころケアセンターにおけるラツーダの使用実態~双極性障害編~

出演・監修:医療法人静心会 桶狭間病院 藤田こころケアセンター
理事長 藤田 潔先生
今回は、藤田 潔先生(医療法人静心会 桶狭間病院 藤田こころケアセンター 理事長)に、桶狭間病院 藤田こころケアセンターにおける双極性障害に対するラツーダの使用実態をご解説いただきます。
理事長 藤田 潔先生
今回は、藤田 潔先生(医療法人静心会 桶狭間病院 藤田こころケアセンター 理事長)に、桶狭間病院 藤田こころケアセンターにおける双極性障害に対するラツーダの使用実態をご解説いただきます。
1.調査概要と患者背景
まず、調査概要を教えてください。

本調査では、実臨床における新規第二世代抗精神病薬ラツーダの治療効果を評価するために、本剤上市直後から双極性障害でラツーダを導入した患者32名を対象とし、年齢、罹病期間、性別、ラツーダの導入状況、投与量、投与期間、中止理由、MADRS(Montgomery Åsberg Depression Rating Scale)、YMRS(Young Mania Rating Scale)スコアの情報を後方視的に調査しました。
なお、前医からラツーダを服用していた患者、頓服のみの患者は評価スケールを用いた有効性の評価から除外しました(図1)。
なお、前医からラツーダを服用していた患者、頓服のみの患者は評価スケールを用いた有効性の評価から除外しました(図1)。


図1
調査対象期間にラツーダを投与されていた双極性障害患者32名の背景を教えてください。

年齢(中央値)は42.0歳、罹病期間(中央値)は9.0年、男女の割合は男性40.6%、女性59.4%でした。
また、ラツーダの投与量(中央値)は40.0mg/日でした。導入方法は、他剤への上乗せが17名(53.1%)、前薬からの切り替えが13名(40.6%)でした(図2,3)。
また、ラツーダの投与量(中央値)は40.0mg/日でした。導入方法は、他剤への上乗せが17名(53.1%)、前薬からの切り替えが13名(40.6%)でした(図2,3)。

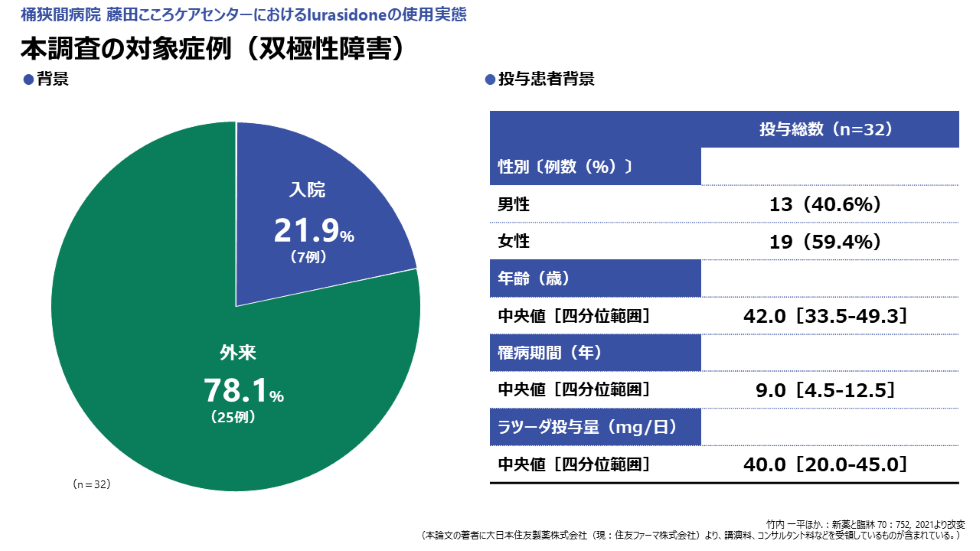
図2

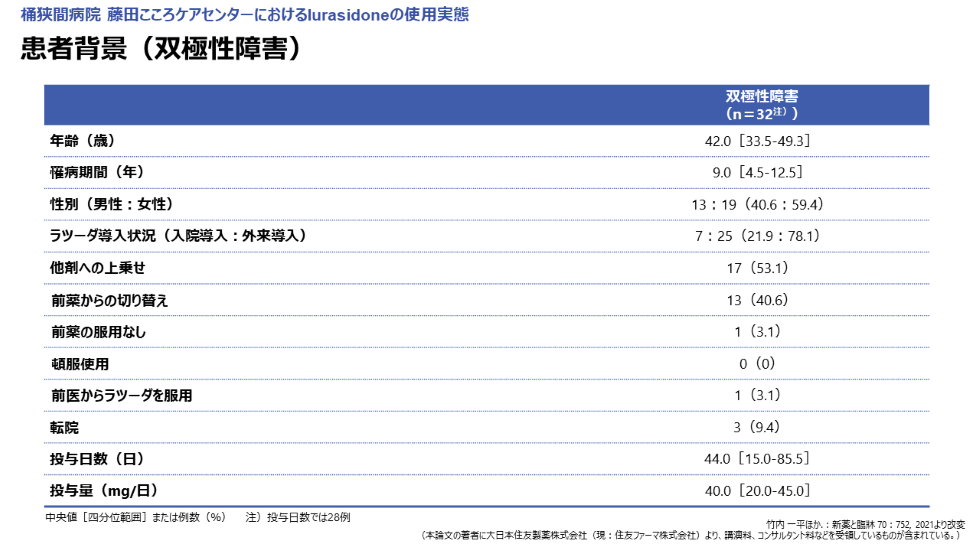
図3
2.MADRSスコア
MADRS合計スコアは、どのように推移したのでしょうか?

MADRS合計スコアの推移はラツーダ投与開始時点の26.8点から開始1週時22.6点、2週時21.2点、4週時17.5点、8週時16.8点と低下し、投与開始時と比べ4、8週時で(p=0.0016, p=0.0025)[名目上のP値] 有意差を認めました(図4)。

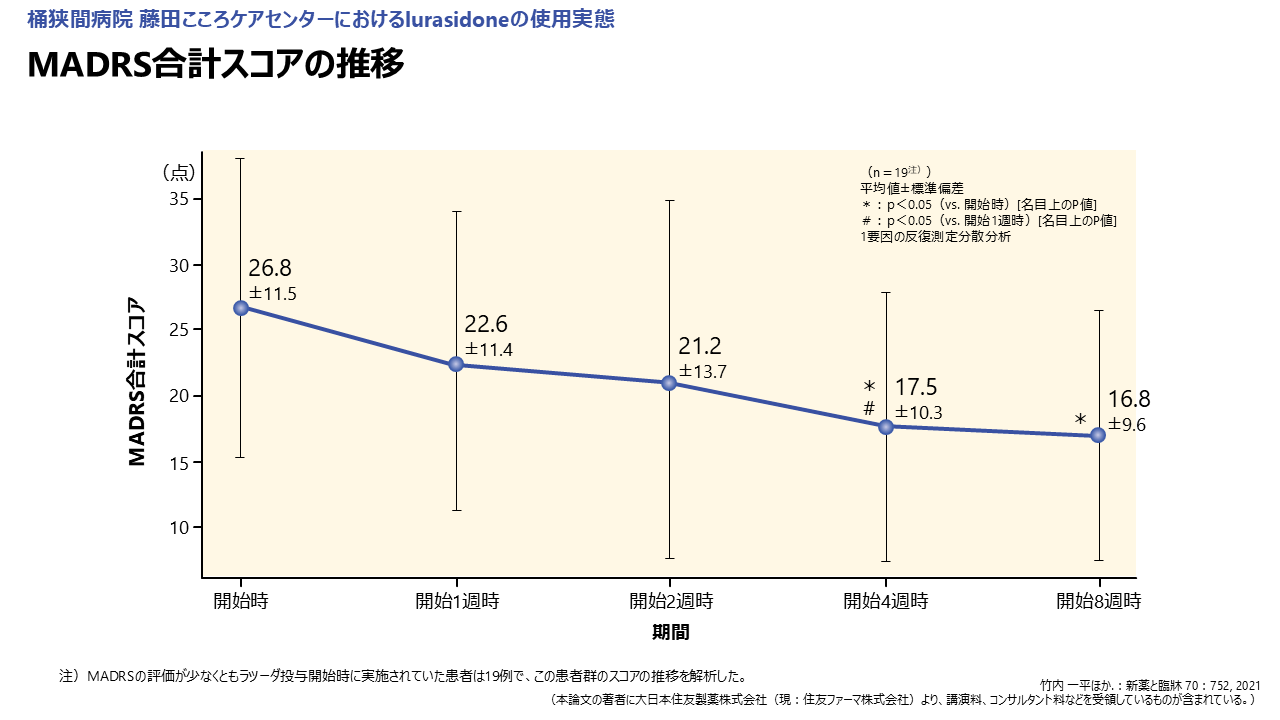
図4
MADRS下位項目についても評価されたのでしょうか?

はい、評価しました。MADRS下位項目の推移及び変化量は、図5,6に示す通りです。投与開始時から8週目のスコア変化量の大きかった項目の上位4つは、言葉で表現された悲しみ(-47.8%)、自殺思考(-45.1%)、外見に表出される悲しみ(-42.9%)、内的緊張(-41.3%)であり、抑うつエピソードの治療で求められるうつの中核症状への効果が実臨床下においても認められました。

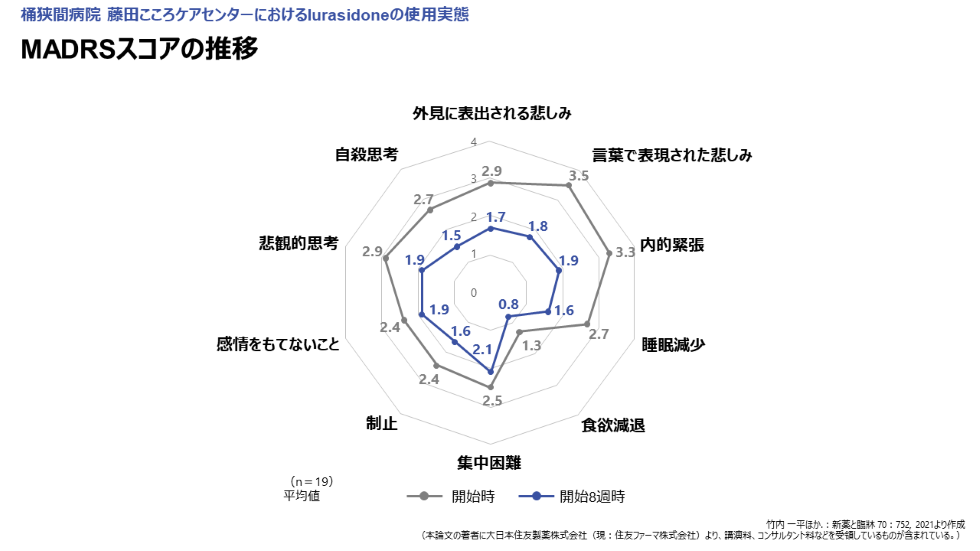
図5

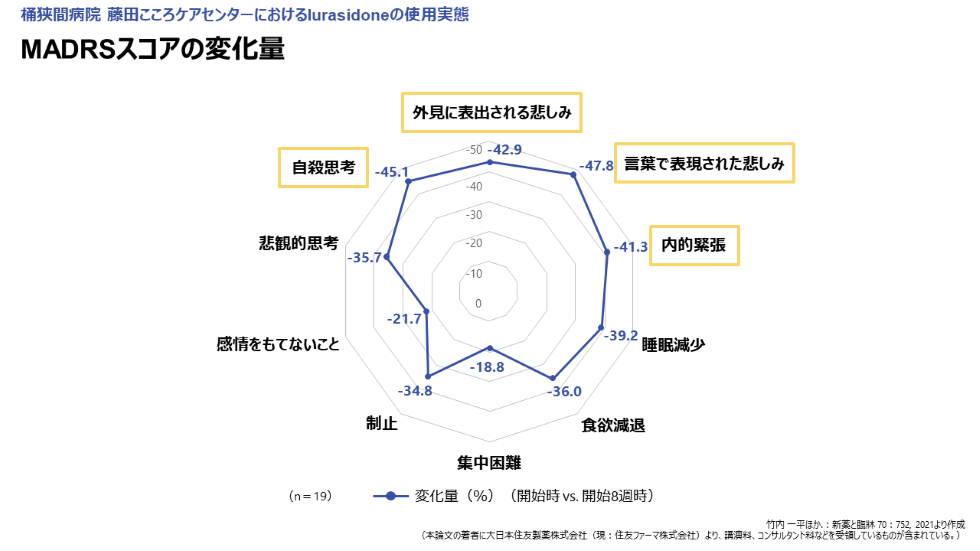
図7
3.投与継続率、中止理由とYMRS合計スコアの推移
ラツーダの投与継続率と、中止理由について教えてください。

投与継続率と中止理由は図7に示す通りです。
中止理由(9名)の内訳は、効果不十分5名、アカシジア1名、本人の意思2名、その他の副作用1名(皮疹)でした。なお、アカシジアが中止の理由となった症例では、発現が確認されてから投与量の減量や抗パーキンソン病薬の投与を行っておらず、発現の確認と同時に投与が中止されていました(図7)。
中止理由(9名)の内訳は、効果不十分5名、アカシジア1名、本人の意思2名、その他の副作用1名(皮疹)でした。なお、アカシジアが中止の理由となった症例では、発現が確認されてから投与量の減量や抗パーキンソン病薬の投与を行っておらず、発現の確認と同時に投与が中止されていました(図7)。

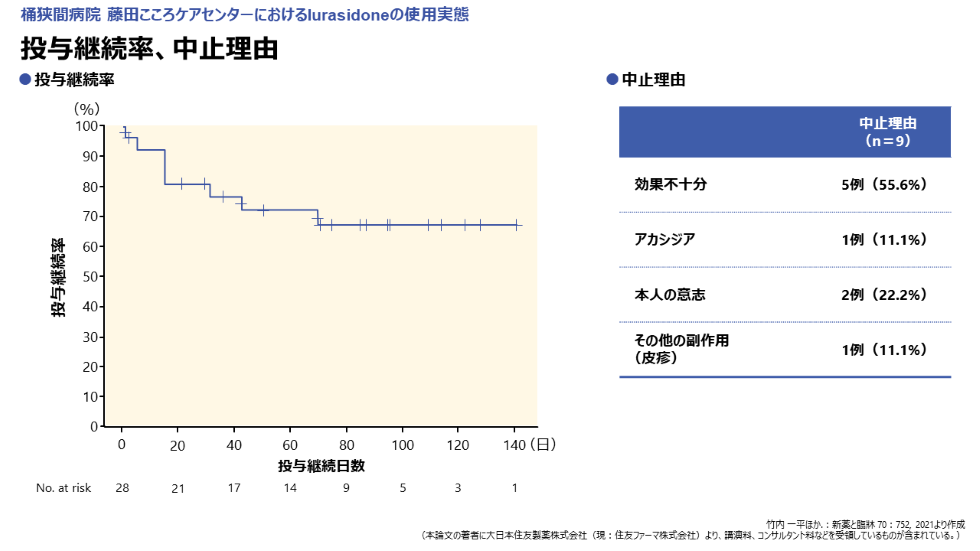
図7
YMRS合計スコアは、どのように推移したのでしょうか?

YMRS合計スコアの推移はラツーダ投与開始時4.6点、開始1週時3.6点、2週時3.6点、4週時3.1点、8週時2.7点と有意な変化は認められませんでした(図8)。

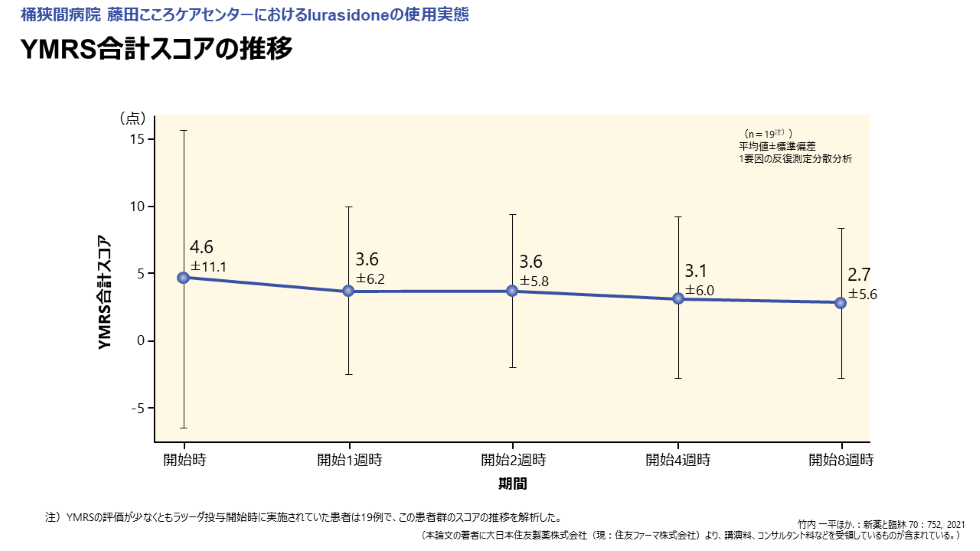
図8
4.考察
本調査をまとめていただけますでしょうか。

MADRSが評価された19例の患者において、MADRS合計スコアの推移は投与開始時26.8点から4週時17.5点、8週時16.8点と開始時と比べて4週時から有意な改善が認められました。
また、YMRS合計スコアの推移はラツーダ投与開始時4.6点、開始1週時3.6点、2週時3.6点、4週時3.1点、8週時2.7点と有意な変化は認められませんでした。
なお、本調査の限界点は図9に示す通りですのでご覧ください。
また、YMRS合計スコアの推移はラツーダ投与開始時4.6点、開始1週時3.6点、2週時3.6点、4週時3.1点、8週時2.7点と有意な変化は認められませんでした。
なお、本調査の限界点は図9に示す通りですのでご覧ください。


図9
最後に、双極性障害を診療されている先生方にメッセージをいただけますか。

本調査では、本邦で初めて実臨床におけるラツーダの双極性障害患者さんへの使用実態を報告しました。これまでに臨床試験で示されていたラツーダの有効性が、当院での使用実態からもお示しできたのではないかと思います。双極性障害患者さんのためのより良い治療に向けて、本日の内容がその一助となれば幸いです。
本邦において双極性障害におけるうつ症状の改善の適応症を取得する根拠となった検証的試験を紹介します。
5.ELEVATE試験
本試験の対象は、双極Ⅰ型障害患者(大うつ病エピソード)525例です。対象をプラセボ群、ラツーダ20-60mg群、ラツーダ80-120mg群に無作為に分け、治験薬を1日1回夕食後に6週間経口投与しました(図10,11)。

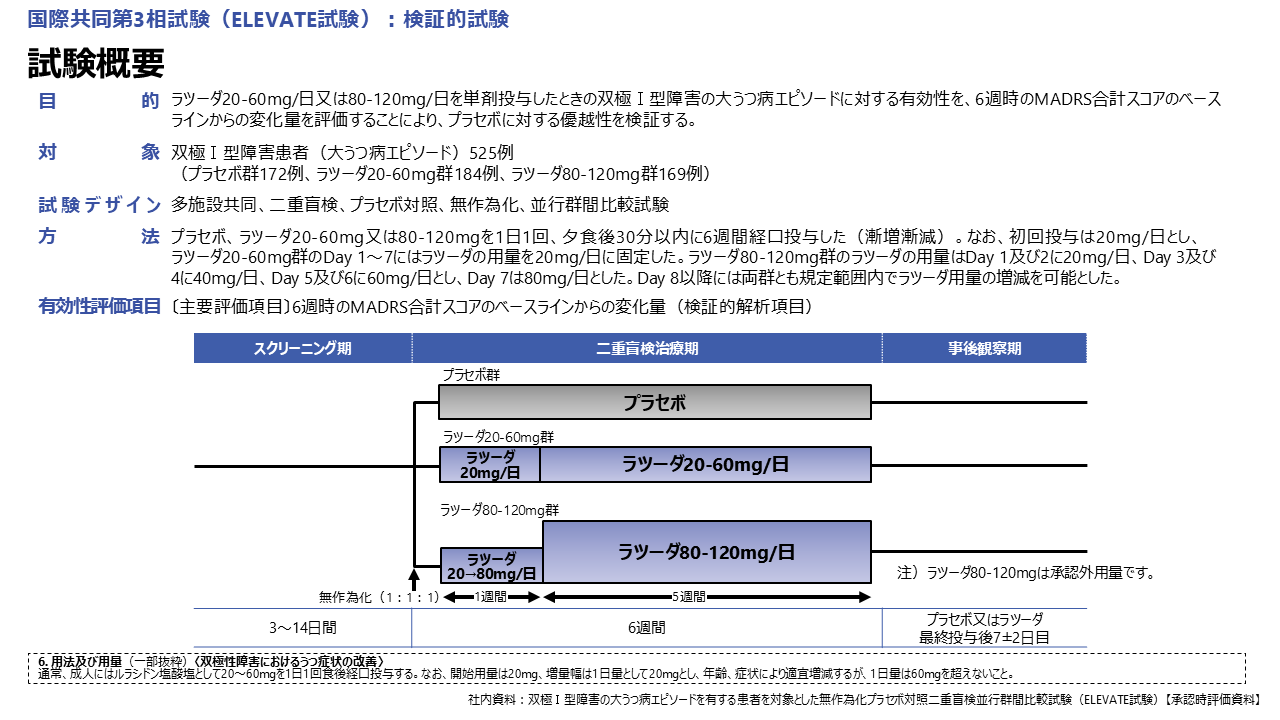
図10


図11
ラツーダ20-60mg群における最頻投与量の割合は20mg/日が37.5%、40mg/日が22.8%、60mg/日が39.7%でした。
また、平均投与量は36.0mgでした。
最終投与量の割合は20mg/日が26.3%、40mg/日が20.6%、60mg/日が53.1%でした(図12)。
また、平均投与量は36.0mgでした。
最終投与量の割合は20mg/日が26.3%、40mg/日が20.6%、60mg/日が53.1%でした(図12)。

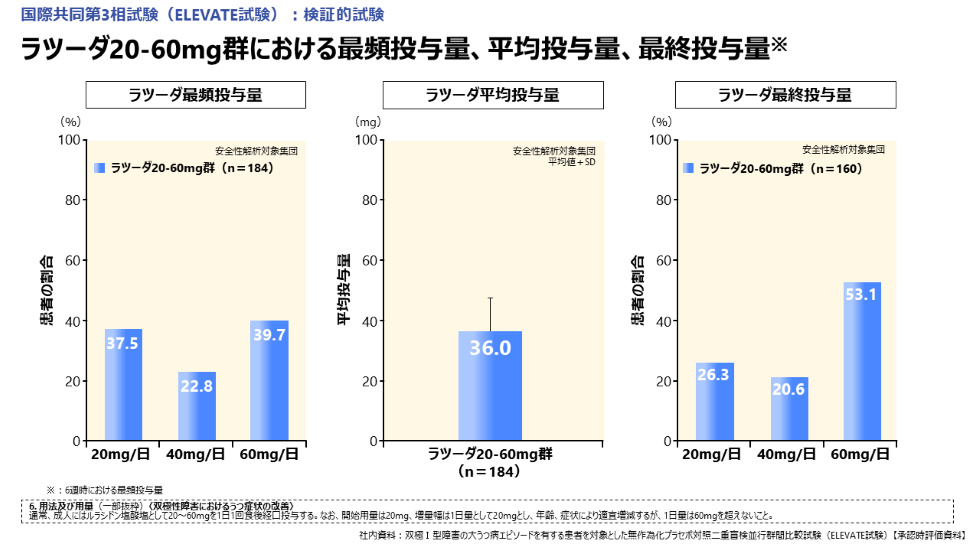
図12
主要評価項目である6週時のMADRS合計スコアのベースラインからの変化量は、プラセボ群−10.6、ラツーダ20-60mg群−13.6、投与群間の差−2.9と、ラツーダ20-60mgはプラセボに比べてMADRS合計スコアを有意に低下させ、プラセボに対する優越性が検証されました。
また、副次評価項目であるベースラインからの変化量は、ラツーダ20-60mg群では投与開始2週目よりプラセボと比べ有意な改善が認められました(図13)
また、副次評価項目であるベースラインからの変化量は、ラツーダ20-60mg群では投与開始2週目よりプラセボと比べ有意な改善が認められました(図13)

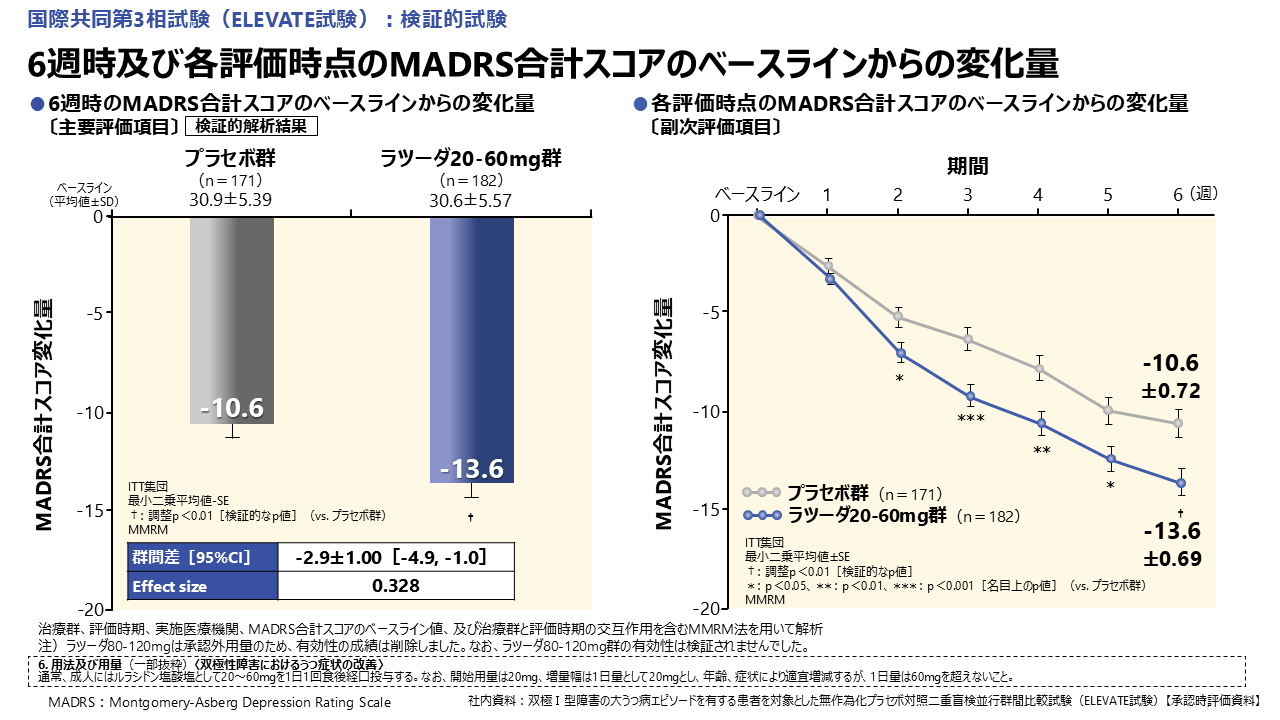
図13
MADRS項目別スコアのベースラインからの変化量をお示しします。うつ症状の中核症状である「外見に表出される悲しみ」や「言葉で表現された悲しみ」など、各項目のスコア変化量はこちらに示すとおりです(図14)。

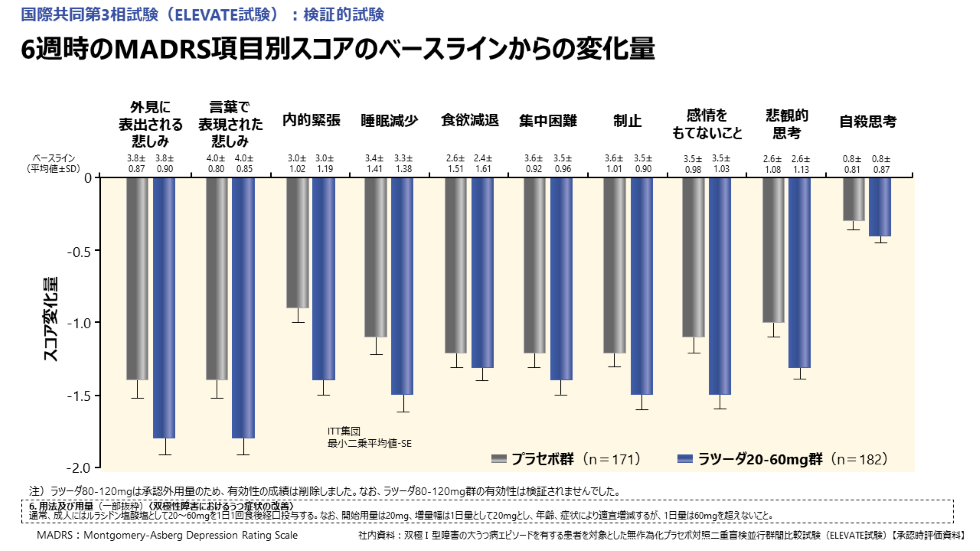
図14
副作用発現率は、プラセボ群55例(32.0%)、ラツーダ20-60mg群71例(38.6%)、ラツーダ80-120mg群87例(51.5%)でした。
発現頻度5%以上の副作用は、プラセボ群ではアカシジア11例(6.4%)、悪心8例(4.7%)、ラツーダ20-60mg群ではそれぞれ24例(13.0%)、12例(6.5%)、ラツーダ80-120mg群ではそれぞれ38例(22.5%)、18例(10.7%)などでした。
重篤な副作用は、プラセボ群1例1件[躁病1件]、ラツーダ20-60mg群0例、ラツーダ80-120mg群2例2件[自殺企図、パニック発作各1件]に認められました。
投与中止に至った有害事象は、プラセボ群7例[好中球減少症、急性心筋梗塞、胃炎、悪心、嘔吐、疾患進行、アカシジア各1例]、ラツーダ20-60mg群6例[嘔吐、機能性胃腸障害、肝障害、アカシジア、躁病、自殺念慮各1例]、ラツーダ80-120mg群16例[悪心4例、疾患進行、アカシジア各3例、嘔吐、腱断裂、筋骨格硬直、ジストニア、不眠症、呼吸困難各1例]に認められました。
試験期間中、いずれの群においても死亡は報告されませんでした(図15)。
発現頻度5%以上の副作用は、プラセボ群ではアカシジア11例(6.4%)、悪心8例(4.7%)、ラツーダ20-60mg群ではそれぞれ24例(13.0%)、12例(6.5%)、ラツーダ80-120mg群ではそれぞれ38例(22.5%)、18例(10.7%)などでした。
重篤な副作用は、プラセボ群1例1件[躁病1件]、ラツーダ20-60mg群0例、ラツーダ80-120mg群2例2件[自殺企図、パニック発作各1件]に認められました。
投与中止に至った有害事象は、プラセボ群7例[好中球減少症、急性心筋梗塞、胃炎、悪心、嘔吐、疾患進行、アカシジア各1例]、ラツーダ20-60mg群6例[嘔吐、機能性胃腸障害、肝障害、アカシジア、躁病、自殺念慮各1例]、ラツーダ80-120mg群16例[悪心4例、疾患進行、アカシジア各3例、嘔吐、腱断裂、筋骨格硬直、ジストニア、不眠症、呼吸困難各1例]に認められました。
試験期間中、いずれの群においても死亡は報告されませんでした(図15)。

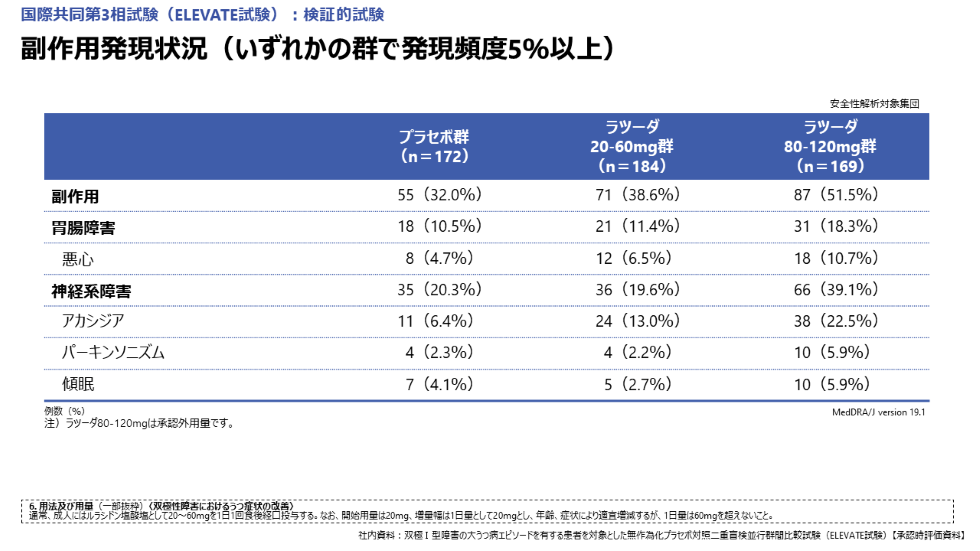
図15
本試験では臨床検査値への影響も検討されています。6週時の体重のベースラインからの変化量は、プラセボ群−0.22kg、ラツーダ20-60mg群0.23kg、ラツーダ80-120mg群0.22kgでした。血糖に関しては、HbA1cが、プラセボ群−0.01%、ラツーダ20-60mg群0.02%、ラツーダ80-120mg群0.02%でした(図16)。

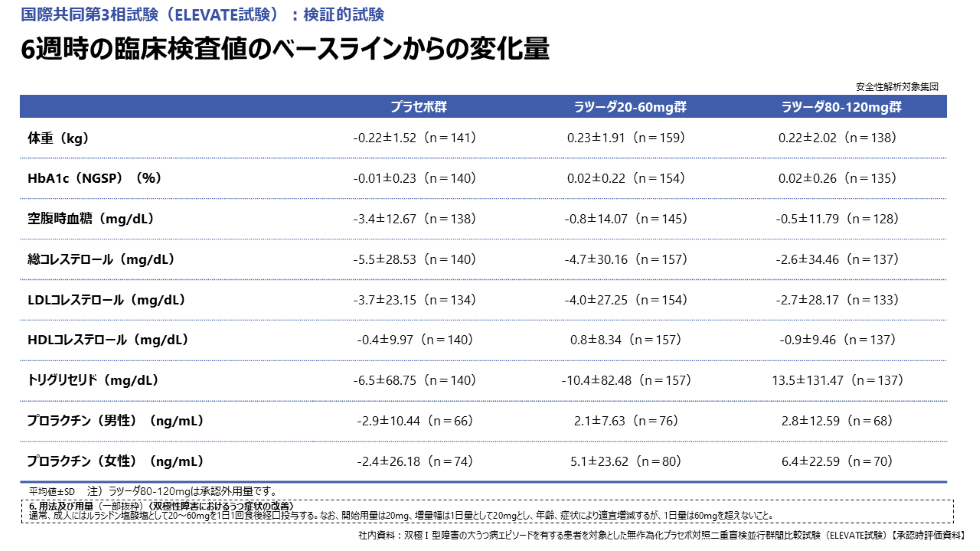
図16

